
以下框图中A~M是中学化学常见的物质,其中A、E是金属,F和J为气体单质,其余均为化合物或其溶液,C为淡黄色固体,D为红棕色粉末,M为红褐色固体。
(1)B的化学式______;
(2)19.5gC与足量的水反应转移电子的物质的量为______mol;
(3)写出物质C的电子式 ;
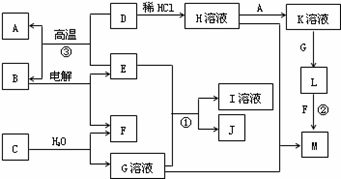 (4)写出②、③反应的离子方程式② ,③ 。
(4)写出②、③反应的离子方程式② ,③ 。
【知识点】框图推断
【答案解析】(1)Al2O3;(2)0.25mol;
(3)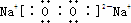 ;
;
(4)②4Fe(OH)2+O2+2H2O = 4Fe(OH)3,
③2Al+Fe2O3 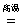 Al2O3 + 2Fe。
Al2O3 + 2Fe。
解析:C为淡黄色固体,能与水反应生成G溶液与F气体单质,故C为Na2O2,G为NaOH,F为O2;
D为红棕色粉末,为Fe2O3,M为红褐色固体,为Fe(OH)3,考虑铝热反应,E为Al,B为Al2O3,电解Al2O3生成Al与O2,符合转化关系,由反应①Al与NaOH溶液反应生成NaAlO2与H2,J为气体单质,故J为H2,I为NaAlO2,代入框图得:A为Fe,K为FeCl2,L为Fe(OH)2 ,(2) 19.5gNa2O2的物质的量为19.5g÷78g/mol=0.25mol,Na2O2完全反应转移电子物质的量为0.25mol1/2×2=0.25mol;(3)Na2O2为离子化合物,电子式为: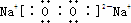 ;
;
【思路点拨】本题借助框图推断考查物质的性质,重点利用了铝热反应、铁的化合物间的转化,这些都是考试的重点。


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
将5.4 g A1投入到200.0 mL 2.0 mol·L-1的某溶液中有氢气产生,充分反应后有金属剩余。该溶液可能为( )。
A.HNO3溶液 B.Ba(OH)2溶液 C.H2SO4溶液 D.HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
向某FeBr2溶液中,通入1.12L(标准状况下)的Cl2,测得溶液中c(Br-)=3c
(Cl-)=0.3mol/L。反应过程中溶液的体积变化忽略不计,则下列说法中正确的是
A.原溶液的浓度约为0.13mol/L B.反应后溶液中c(Fe3+)=0.1mol/L
C.反应后溶液中c(Fe3+)=c(Fe2+) D.原溶液中c(Br-)= 0.4mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
关于右图所示装置(盐桥含KCl)的叙述,正确的是
A.铜离子在铜片表面被氧化
B.铜作阳极,铜片上有气泡产生
C.电流从锌片经导线流向铜片
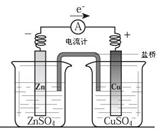 D.右侧烧杯中,SO42-的物质的量几乎不变,K+的数目增多
D.右侧烧杯中,SO42-的物质的量几乎不变,K+的数目增多
查看答案和解析>>
科目:高中化学 来源: 题型:
相同条件下,0.1mol/L Na2S2O3溶液和0.1mol/L H2SO4溶液各5mL,与10mL水混合,反应时间为t1 s;0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,反应时间为t2 s,则t1和t2的关系是(忽略体积变化)
A. t1>t2 B. t1<t2 C. t1=t2 D.不能肯定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体的叙述中不正确的是
A.布朗运动是胶体微粒特有的运动方式,只用肉眼就可以把胶体和溶液、浊液区别开来
B.向Fe(OH)3胶体中加入少量H2SO4溶液,会生成红褐色沉淀
C.丁达尔效应是胶体的特性
D.胶体微粒具有较大的表面积,能吸附阳离子或阴离子,故在电场作用下会产生电泳现象
查看答案和解析>>
科目:高中化学 来源: 题型:
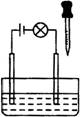
在电解质溶液的导电性装置(如右图所示)中,若向某一电解质溶液中逐滴加入另一溶液,则灯泡由亮变暗至熄灭,后又逐渐变亮的是
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入NaOH溶液
C.硫酸中逐滴加入Ba(OH)2溶液
D.硫酸铜溶液中逐滴加入NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
铝镁合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用作窗框、卷帘门、防护栏等。下列与这些用途无关的性质是( )。
A.不易生锈 B.导电性好 C.密度小 D.强度高
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.锅炉中沉积的CaSO4可用Na2CO3溶液浸泡后,再将不溶物用稀盐酸溶解去除
B.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进了Fe3+水解
C.向纯水中加入盐酸或降温都能使水的离子积减小,电离平衡逆向移动
D.反应2A(g)+B(g)===3C(s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com