
【题目】人体内缺乏维生素A会使人患夜盲症,原因是维生素A在人体内易被氧化为视黄醛,而视黄醛的缺乏是引起视觉障碍的主要原因。已知视黄醛结构为:

(1)检验分子中醛基的方法是____反应。操作方法____,则证明原溶液中有醛基。
(2)检验分子中碳碳双键的方法是____。
(3)实验中先检验哪种官能团?____试简述理由____。
【答案】银镜 加入银氨溶液,水浴加热,有光亮的银镜生成 加入溴水,振荡,溴水褪色 醛基 溴水为强氧化剂,能够将-CHO氧化为羧基
【解析】
(1)醛具有较强的还原性,能被新制的银氨溶液氧化为羧酸;
(2)碳碳双键能与溴水发生加成反应;
(3)视黄醛的分子结构中有碳碳双键和醛基,无论哪一种官能团,都可使溴水褪色,据此分析解答。
(1)醛具有较强的还原性,能被新制的银氨溶液氧化为羧酸,同时Ag(NH3)2OH被还原为Ag,若控制好反应条件,可以得到光亮的银镜,故答案为:银镜;加入银氨溶液,水浴加热,有光亮的银镜生成;
(2)碳碳双键能与溴水发生加成反应,使溴水褪色,故答案为:加入溴水,振荡,溴水褪色;
(3)视黄醛的分子结构中有碳碳双键和醛基,银氨溶液为弱氧化剂,不能氧化碳碳双键,但溴水为强氧化剂,-CHO也可以将其还原,故检验碳碳双键时应先将-CHO氧化,再加溴水检验碳碳双键,故答案为:醛基;溴水为强氧化剂,能够将-CHO氧化为羧基。


科目:高中化学 来源: 题型:
【题目】四种短周期元素在周期表中的位置如图所示,其中只有M为金属元素。下列说法不正确的是( )
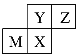
A.原子半径:Z<M
B.Y的最高价氧化物对应水化物的酸性比X的弱
C.X的最简单气态氢化物的热稳定性比Z的小
D.Z位于元素周期表中第二周期ⅤA族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用可逆反应N2(g)+3H2(g) ![]() 2NH3(g)合成氨,下列叙述正确的是( )
2NH3(g)合成氨,下列叙述正确的是( )
A.合成氨的适宜条件是高温高压催化剂,其中催化剂不改变该反应的逆反应速率
B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为: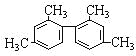 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有11个碳原子处于同一平面上
C.分子中至少有16个碳原子处于同一平面上
D.该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物甲(如图所示)中所有原子都达到了 8电子稳定结构,X、Y、Z、W是原子序数依次增大的短周期主族元素,原子半径:r(w)> r(X)> r(Y) > r(Z)。下列说法正确的是( )
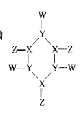
A.YZ,属于酸性氧化物
B.元素的非金属件强弱:Y>Z
C.X的最高价氢化物对应的水化物是强酸
D.Y的最简单氢化物能与W的氢化物反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2(g)+ ![]() O2(g)=H2O(g);ΔH1= akJ·mol-1
O2(g)=H2O(g);ΔH1= akJ·mol-1
②2H2(g)+O2(g) = 2H2O(g);ΔH2= b kJ·mol-1 ③ H2(g)+ ![]() O2(g)=H2O(l);ΔH3= c kJ·mol-1
O2(g)=H2O(l);ΔH3= c kJ·mol-1
④2H2(g)+O2(g) = 2H2O(l);ΔH4= d kJ·mol-1,下列关系式中正确的是( )
A.2a=b<0B.b>d>0C.a<c<0D.2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:AgBr比AgCl更难溶,将AgCl与AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,发生的反应为
A. 只有AgBr沉淀生成 B. AgCl与AgBr沉淀等量生成
C. AgCl与AgBr沉淀都有,但以AgCl沉淀为主 D. AgCl与AgBr沉淀都有,但以AgBr沉淀为主
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习小组进行如下实验。
【探究反应速率的影响因素】设计了如下的方案并记录实验结果(忽略溶液混合体积变 化)。限选试剂和仪器:0.20mol/LH2C2O4 溶液、0.010mol/L KMnO4 溶液(酸性)、蒸馏水、 试管、量筒、秒表、恒温水浴槽
(1)上述实验①②是探究 对化学反应速率的影响;若上述实验②③是探究浓度对化学反应速率的影响,则 a 为 ;乙是实验需要测量的物理量,则表 格中“乙”应填写 。
【测定 H2C2O4·xH2O 中 x 值】 已知:M(H2C2O4)=90g/mol
称取 1.260 g 纯草酸晶体,将其酸制成 100.00 mL 水溶液为待测液。
②取 25.00 mL 待测液放入锥形瓶中,再加入适的稀 H2SO4
③用浓度为 0.05000 mol·L-1 的 KMnO 标准溶液进行滴定;
(2)请写出与滴定有关反应的离子方程式
(3)某学生的滴定方式(夹持部分略去)如下,最合理的是 (选填 a、b)。


(4)由右图可知消耗 KMnO4 溶液体积为 mL;
(5)滴定过程中眼睛应注视_________________;
(6)通过上述数据,求得 x= 。以标准 KMnO4 溶液滴定样品溶液的浓度,未用 标准 KMnO4 溶液润洗滴定管,引起实验结果 (偏大、偏小或没有影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸乙酯广泛用于药物、染料、香料等工业,中学化学实验常用a装置来制备。
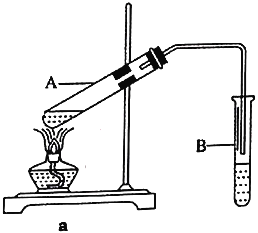
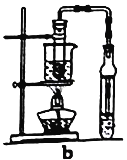
完成下列填空:
(1)实验中用到的三种试剂添加的先后顺序是____________________________。
(2)a装置中试管B中试剂的作用是________________________________________。
(3)实验时,通常加入过量的乙醇,原因是________________________________________。
(4)加入数滴浓硫酸即能起催化作用,但实际用量多于此量,原因是_______________________;浓硫酸用量又不能过多,原因是______________________________________________。
(5)反应结束后,将B试管中收集到的产品倒入分液漏斗中,______________、_____________,然后分液。
(6)若用b装置制备乙酸乙酯,其优点有____________、_____________。由b装置制得的乙酸乙酯产品经饱和碳酸钠溶液和饱和食盐水洗涤后,还可能含有的有机杂质是________________,分离乙酸乙酯与该杂质的方法是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com