
【题目】已知NO不溶于水,NO2易溶于水,且与水发生反应3NO2+H2O═2HNO3+NO.有48mL NO和NO2混合气体的容器倒置于水中(保持同温同压),待液面稳定后,容器内气体的体积变为24 mL,则:
(1)原混合气中,NO是mL,NO2是mL.
(2)若在剩余的24mL气体中,通入6mL O2 , 待液面稳定后,反应后容器内剩余气体体积为mL.
(3)若在剩余的24mL气体中,通入24mL O2 , 待液面稳定后,反应后容器内剩余气体体积为mL.
(4)若在原48mL NO,NO2中,通入mL O2再倒置于水中,气体会全部被吸收.
【答案】
(1)12;36
(2)16
(3)6
(4)18
【解析】解:(1)一氧化氮和水不反应,二氧化氮和水能反应,反应方程式为:3NO2+H2O=2HNO3+NO,
设二氧化氮的体积为x,
3NO2 | +H2O=2HNO3+ | NO | 气体体积减少 |
3 | 2 | ||
x | (48﹣24)mL=24mL |
x= ![]() =36mL,
=36mL,
则一氧化氮体积=(48﹣36)mL=12mL,
NO体积是 12mL,二氧化氮体积是NO2 36 mL,
所以答案是:12;36;(2)剩余气体是一氧化氮,一氧化氮、氧气和水之间的反应式为:4NO+3O2+2H2O=4HNO3 ,
根据方程式知,一氧化氮和氧气反应的关系是4:3,则有24mL一氧化氮反应时需要18mL氧气,实际上有6mL氧气,所以一氧化氮有剩余,剩余的一氧化氮体积=24mL﹣ ![]() ×4=16mL,
×4=16mL,
所以答案是:16;(3)由4NO~3O2知,24 mLNO消耗O2的体积为: ![]() ×24mL=18mL,所以反应后容器内剩余O2为:24 mL﹣18 mL=6 mL,
×24mL=18mL,所以反应后容器内剩余O2为:24 mL﹣18 mL=6 mL,
所以答案是:6;
·(4)由
4NO+ | 3O2 | +2H2O═4HNO3 |
4 | 3 | |
36mL | 9mL | |
4NO2+ | O2 | +2H2O═4HNO3 |
4 | 3 | |
36mL | 9mL |
则需要通入18 mL O2 , 可使管内气体全部被H2O吸收,
所以答案是:18.


科目:高中化学 来源: 题型:
【题目】图中A,B,C,D是同周期或同主族的相邻元素: ![]()
(1)已知:A元素的最低价为﹣3价,它的最高价氧化物含氧56.34%,原子核内中子数比质子数多1个,则A元素原子的质量数为 .
(2)写出元素符号A , C , D .
(3)A,B,C三种元素最高价氧化物的水化物中酸性最强的是 . (填化学式)
(4)B,D两种元素和氢组成的气态氢化物中稳定性强的是 , 还原性最强的是(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用最主要的能源。
(1)化学反应中放出的热能(焓变,ΔH)与反应物和生成物的键能(E)有关。已知:
①H2(g)+Cl2(g)=2HCl(g) ΔH=-a ![]()
②E(H-H)=b![]() , E(Cl-Cl)=c
, E(Cl-Cl)=c ![]()
则:E(H-Cl)=_____________kJ·mol-1。
(2)实验中不能直接测出由石墨和氢气反应生成甲烷反应的反应热,但可测出CH4、石墨和H2燃烧反应的反应热,求由石墨生成甲烷的反应热。已知:
①CH4(g)+2O2(g)==CO2(g)+2H2O(l) △H=-a kJ·mol-1
②C(石墨)+O2(g)==CO2(g) △H=-b kJ·mol-1
③H2(g)+1/2O2(g)==H2O(l) △H=-c kJ·mol-1
则反应C(石墨)+2H2(g) → CH4(g)的反应热△H=________kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列与NA有关的说法正确的是
A. 12g金刚石中含有的共价键数为4NA
B. S2和S8的混合物共64 g,其中所含硫原子数—定为2NA
C. 60gSiO2晶体中含有Si-O键数目为2NA
D. 44g干冰晶胞( )含有的CO2分子个数为14NA
)含有的CO2分子个数为14NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铜在常温下能被HNO3溶解,反应方程式为:3Cu+8HNO3═3Cu(NO3)2+2NO↑+4H2O
(1)请将上述反应改成离子方程式
(2)上述反应中,氧化剂是 , 氧化产物是 .
(3)每2molCu参加反应,转移的电子个,在反应的硝酸中没有参加氧化还原反应的硝酸占总硝酸的 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】想一想:Ba(OH)2(固体)、CuSO4(固体)、CH3COOH(液态)这些物质为什么归为一类,下列哪些物质还可以和它们归为一类
A、75%的酒精溶液 B、硝酸钠
C、Fe(OH)3胶体 D、豆浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是( )
A. 碳酸钙与盐酸反应: CaCO3+2H+===CO2↑+H2O+ Ca2+
B. 硫酸和氢氧化钡溶液反应: 2OH- + Ba2++2H++SO![]() ===BaSO4↓+2H2O
===BaSO4↓+2H2O
C. 铁钉放入硫酸铜溶液中: 2Fe+3Cu2+===2Fe3++3Cu
D. 钠与水反应: 2Na+2H2O ===2Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
Q、R、X、Y、Z为周期表前四周期元素,原子序数依次递增。已知:
①Q为元素周期表中原子半径最小的元素;
②R的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;
③Y的基态原子的核外成对电子数是未成对电子数的3倍;
④Q、R、Y三种元素组成的一种化合物M是新装修居室中常含有的一种有害气体,Q、R两种元素组成的原子个数比为1:1的化合物N是中学化学中常见的有机溶剂;
⑤Z有“生物金属”之称,Z4+离子和氩原子的核外电子排布相同。
请回答下列问题(答题时,Q、R、X、Y、Z用所对应的元素符号表示)
(1)化合物M的空间构型为______________ ,其中心原子采取_________杂化;化合物N在固态时的晶体类型为_______________。
(2)R、X、Y三种元素的第一电离能由小到大的顺序为___________。
(3)由上述一种或多种元素组成的与RY2互为等电子体的分子为__________(写分子式)。
(4)由R、X、Y三种元素组成的RXY-离子在酸性条件下可与NaClO溶液反应,生成X2、RY2等物质。该反应的离子方程式为______________________________。
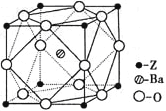
(5)Z原子基态时的外围电子排布式为_________________;Z的一种含氧酸钡盐的晶胞结构如图所示,晶体内与每个Z原子等距离且最近的氧原子数为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com