
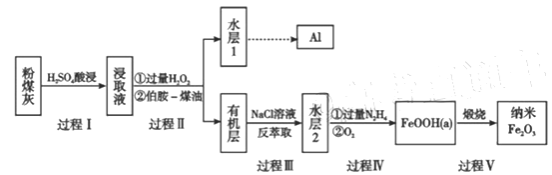
【题目】粉煤灰是燃煤产生的重要污染物,主要成分有Al2O3、Fe2O3、Fe3O4和SiO2等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米Fe2O3等重要物质。
已知:
i)伯胺R-NH2能与Fe3+反应;3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
ii)Fe3+在水溶液中能与Cl-反应:Fe3++6Cl-![]() [FeCl6]3-,回答下列问题:
[FeCl6]3-,回答下列问题:
(1)过程I对煤粉灰进行酸浸过滤后,滤渣的主要成分是_________。
(2)写出过程II加入过量H2O2发生的离子方程式_________。加入伯胺-煤油对浸取液进行分离,该操作的名称是_________。
(3)从化学平衡角度解释过程III利用NaCl溶液进行反萃取的原理________。
(4)过程IV中过量的N2H4将水层2中[FeCl6]3-转化为Fe2+,得到的Fe2+再被O2氧化为FeOOH,其中第一步的离子方程式为4[FeCl6]3-+5N2H4=4Fe2++N2+.4N2H5++24Cl-,该反应中氧化剂与还原剂的物质的量之比为_________。
(5)在常压用纳米Fe2O3电化学法合成氨的装置如图所示。
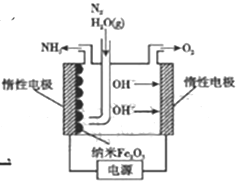
已知电解液为熔融NaOH-KOH,纳米Fe2O3在阴极发生电极反应分两步进行:该电解池第二步:2Fe+N2+3H2O=Fe2O3+2NH3。则该电解池第一步发生反应的方程式为_________。纳米Fe2O3在电解过程中所起的作用是_______。
【答案】SiO2 2Fe2++H2O2+2H+=2Fe3++2H2O 萃取、分液 Fe3++6Cl-![]() [FeCl6]3-(已知ⅱ中的反应),导致Fe3+浓度降低,使3R-NH2+Fe3++SO42-+H2O
[FeCl6]3-(已知ⅱ中的反应),导致Fe3+浓度降低,使3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+(已知ⅰ中的反应),平衡向逆反应方向移动,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,实现反萃取。 4:1 Fe2O3+3H2O+6e-=2Fe+6OH- 催化剂
Fe(NH2-R)3(OH)SO4+H+(已知ⅰ中的反应),平衡向逆反应方向移动,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,实现反萃取。 4:1 Fe2O3+3H2O+6e-=2Fe+6OH- 催化剂
【解析】
粉煤灰主要成分有Al2O3、Fe2O3、Fe2O4和SiO2等物质,过程Ⅰ酸浸,二氧化硅不溶于硫酸,除去二氧化硅;浸取液中含有Fe2+、Fe3+、Al3+,加入过氧化氢与Fe2+发生氧化还原反应生成Fe3+,再加入伯胺R-NH2与Fe3+反应;3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物,得到有机层。对有机层进行反萃取操作,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,再经过系列操作得到纳米三氧化二铁。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物,得到有机层。对有机层进行反萃取操作,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,再经过系列操作得到纳米三氧化二铁。
(1)过程I对煤粉灰进行酸浸,主要成分二氧化硅不溶于酸,故过滤后滤渣的主要成分是SiO2。
(2)过程II加入过量H2O2与Fe2+发生氧化还原反应生成Fe3+,离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O。加入伯胺-煤油对浸取液进行分离,得到有机层和水层1,该操作的名称是萃取、分液。
(3)Fe3++6Cl-![]() [FeCl6]3-(已知ⅱ中的反应),导致Fe3+浓度降低,使3R-NH2+Fe3++SO42-+H2O
[FeCl6]3-(已知ⅱ中的反应),导致Fe3+浓度降低,使3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+(已知ⅰ中的反应),平衡向逆反应方向移动,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,实现反萃取。
Fe(NH2-R)3(OH)SO4+H+(已知ⅰ中的反应),平衡向逆反应方向移动,Fe3+从易溶于煤油的物质中转化到易溶于水的物质中,实现反萃取。
(4)4[FeCl6]3-+5N2H4=4Fe2++N2+4N2H5++24Cl-中,铁元素化合价降低,[FeCl6]3-作氧化剂,氮元素化合升高,N2H4作还原剂,但并不是所有参与反应的N2H4都作还原剂,5mol N2H4反应只有1mol作还原剂,故该反应中氧化剂与还原剂的物质的量之比为4:1。
(5)该装置为电解装置,阴极发生还原反应,总电极反应为N2+6e-+6H2O=2NH3+6OH-,已知阴极发生电极反应分两步进行,第二步:2Fe+N2+3H2O=Fe2O3+2NH3,则该电解池第一步发生反应的方程式为Fe2O3+3H2O+6e-=2Fe+6OH-。纳米Fe2O3在电解过程中质量和性质未发生改变,故其所起的作用是催化剂。


科目:高中化学 来源: 题型:
【题目】氨是重要的基础化工原料,可以制备尿素[CO(NH2)2]、N2H4等多种含氮的化工产品。
(1)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g)![]() NH2CO2NH4(s) △H1= -159.5kJ·mol-1
NH2CO2NH4(s) △H1= -159.5kJ·mol-1
反应II:NH2CO2NH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1
CO(NH2)2(s)+H2O(g) △H2=+116.5kJmol-1
反应III:H2O(l)=H2O(g) △H3=+44.0kJmol-1
则反应:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(l) △H=______kJmol-1
CO(NH2)2(s)+H2O(l) △H=______kJmol-1
(2)将氨气与二氧化碳在有催化剂的反应器中反应2NH3(g)+CO2(g)![]() CO(NH2)2 (s)+H2O(g),体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
CO(NH2)2 (s)+H2O(g),体系中尿素的产率和催化剂的活性与温度的关系如图1所示:
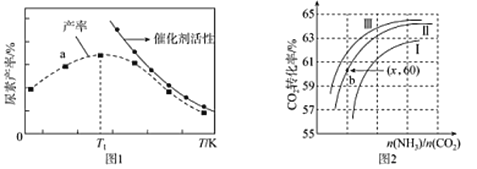
①a点_______(填是或不是)处于平衡状态,Tl之后尿素产率下降的原因是________。
②实际生产中,原料气带有水蒸气,图2表示CO2的转化率与氨碳比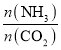 、水碳比
、水碳比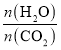 的变化关系。曲线I、II、III对应的水碳比最大的是_______,测得b点氨的转化率为30%,则x=___________。
的变化关系。曲线I、II、III对应的水碳比最大的是_______,测得b点氨的转化率为30%,则x=___________。
③已知该反应的v(正)=k(正)c2(NH3)c(CO2),v(逆)=k(逆)c(H2O),k(正)和k(逆)为速率常数,则平衡常数K与k(正)、k(逆)的关系式是___________。
(3)N2H4可作火箭推进剂。已知25℃时N2H4水溶液呈弱碱性:N2H4+H2O![]() N2H5++OH- K1=1×10-a;N2H5++H2O
N2H5++OH- K1=1×10-a;N2H5++H2O![]() N2H62++OH- K2=1×10一b。
N2H62++OH- K2=1×10一b。
①25 ℃时,向N2H4水溶液中加入H2SO4,欲使c(N2H5+)>c(N2H4),同时c(N2H5+)>c(N2H62+),应控制溶液pH范围__________(用含a、b式子表示)。
②水合肼(N2H4H2O)的性质类似一水合氨,与硫酸反应可以生成酸式盐,该盐的化学式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,两电极一为碳棒,一为铁片,若电流表的指针发生偏转,且a极上有大量气泡生成,则以下叙述正确的是

A. a为负极,是铁片,烧杯中的溶液为硫酸
B. b为负极,是铁片,烧杯中的溶液为硫酸铜溶液
C. a为正极,是碳棒,烧杯中的溶液为硫酸
D. b为正极,是碳棒,烧杯中的溶液为硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10mL0.1mol·L-1一元弱碱XOH溶液中逐滴滴加0.1mol·L-1的HCl溶液,溶液的AG![]() 变化如图所示(溶液混合时体积变化忽略不计)。下列说法不正确的是
变化如图所示(溶液混合时体积变化忽略不计)。下列说法不正确的是
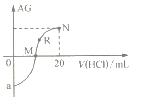
A. 若a=-8,则Kb(XOH)≈10-5
B. M点表示盐酸和XOH恰好完全反应
C. R点溶液中可能存在c(X+)+c(XOH)=c(Cl-)
D. M点到N点,水的电离程度先增大后减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.56gCu和一定量的浓HNO3反应,随着Cu的不断减少,反应生成气体的颜色逐渐变浅,当Cu反应完毕时,共收集到气体1.12L(标准状况),则反应中消耗HNO3的物质的量为
A.0.05molB.0.13molC.1molD.1.05mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平。A在一定条件下可以合成聚合物B,B可作食品包装袋。请回答下列问题:
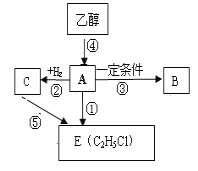
(1)A的结构简式是_________;反应③的反应类型为:____________ 。
(2)写出反应③、④的化学方程式反应③:________________________________________;
反应④:_________________________________________;
(3)乙烯作为重要的有机原料,工业上常用来制取乙醇,试写出该反应的化学方程式_____________。
(4)乙醇作为重要的有机原料,可以制取乙醛、乙醚等重要的有机物,试写出乙醇催化氧化制取
乙醛的化学方程式___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列金属冶炼的反应原理,不正确的是
A.2Ag2O![]() 4Ag+O2↑B.Fe2O3+3CO
4Ag+O2↑B.Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
C.6MgO+4Al![]() 6Mg+2Al2O3D.2NaCl(熔融)
6Mg+2Al2O3D.2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作和现象、结论都正确的是( )
选项 | 实验操作和现象 | 实验结论 |
A | 常温下,将大小、形状形态的锌和铝分别加入到等体积 | 锌比铝活泼 |
B | 向某溶液中加入盐酸酸化的氯化钡溶液,产生白色沉淀 | 该溶液中一定含有 |
C | 将盐酸滴入碳酸钠溶液中,产生气泡 | 非金属性:Cl大于C |
D | 向某溶液中加入氢氧化钠溶液丙加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中一定含有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[Cu(NH3)4]SO4是一种深蓝色的配位化合物。
(1)Cu2+可被还原成Cu+,Cu+基态核外的外围电子排布式为_________________________。
(2)H元素与N元素可形成分子式为N2H2的化合物,该物质的分子具有平面结构,则该分子中N原子的杂化轨道类型为______________________。
(3)与CS2分子互为等电子体的SCN-离子的电子式为_________________。
(4)Cu可形成多种配合物,且各种配合物有广乏的用途。某Cu的配合物结构如图1所示,则该配合物中心原子Cu的配体数为____;其分子内含有的作用力有________(填序号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位健
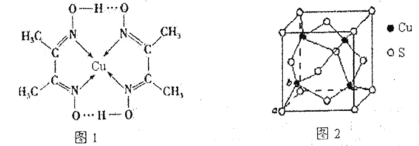
(5)Cu元素与S元素形成的一种化合物品跑如图2所示,其中S的配位数为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com