
【题目】有机物A是一种重要的化工原料,A的产量可以用来衡量一个国家的石油化工水平。A在一定条件下可以合成聚合物B,B可作食品包装袋。请回答下列问题:
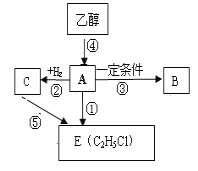
(1)A的结构简式是_________;反应③的反应类型为:____________ 。
(2)写出反应③、④的化学方程式反应③:________________________________________;
反应④:_________________________________________;
(3)乙烯作为重要的有机原料,工业上常用来制取乙醇,试写出该反应的化学方程式_____________。
(4)乙醇作为重要的有机原料,可以制取乙醛、乙醚等重要的有机物,试写出乙醇催化氧化制取
乙醛的化学方程式___________________________________________。
【答案】CH2=CH2 加聚反应 nCH2=CH2![]()
![]() CH3CH2OH
CH3CH2OH![]() CH2 = CH2↑+ H2O CH2 = CH2 + H2O
CH2 = CH2↑+ H2O CH2 = CH2 + H2O![]() CH3CH2OH 2CH3CH2OH+O2
CH3CH2OH 2CH3CH2OH+O2![]() 2CH3CHO + 2H2O
2CH3CHO + 2H2O
【解析】
有机物A 的产量可以用来衡量一个国家的石油化工水平,则A为CH2=CH2;A在一定条件下可以合成聚合物B,B可作食品包装袋,则B为![]() ;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,据此进行解答.
;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl,据此进行解答.
有机物A 的产量可以用来衡量一个国家的石油化工水平,则A为CH2=CH2;A在一定条件下可以合成聚合物B,B可作食品包装袋,则B为![]() ;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl;
;根据图示可知,乙烯与氢气反应生成C,则C为CH3CH3;C通过反应⑤生成E,则E为CH3CH2Cl;
(1)A为乙烯,其结构简式为CH2=CH2;反应③为乙烯转化成聚乙烯,该反应为加聚反应;
(2)③为乙烯发生加聚反应生成聚乙烯,反应的化学方程式为n CH2=CH2![]()
![]() ;④为乙醇在浓硫酸作用下加热到170℃时发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH
;④为乙醇在浓硫酸作用下加热到170℃时发生消去反应生成乙烯,反应的化学方程式为:CH3CH2OH![]() CH2 = CH2↑+ H2O;
CH2 = CH2↑+ H2O;
(3)乙烯与水发生加成反应生成乙醇,发生反应的化学方程式为CH2 = CH2 + H2O![]() CH3CH2OH;
CH3CH2OH;
(4)乙醇催化氧化生成乙醛的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO + 2H2O。
2CH3CHO + 2H2O。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法不正确的是
A.常温常压下,2 g D2O 中含中子数为NA
B.1mol苯乙烯(![]() )分子中含有碳碳双键的个数为4 NA
)分子中含有碳碳双键的个数为4 NA
C.0.5mol羟基中所含电子数为4.5NA
D.28g乙烯和丙烯(C3H6)的混合气体含有的碳原子数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】单质硼有无定形和晶体两种,参考下表数据回答:
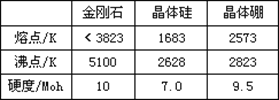
(1)晶体硼的晶体类型属于____________________晶体,理由是_____________ 。
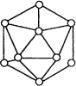
(2)已知晶体的结构单元是由硼原子组成的正二十面体(如图),其中有20个等边三角形的面和一定数目的顶角,每个顶角各有一个硼原子。通过观察图形及推算,得出此基本结构单元是由__________个硼原子构成的,其中B—B键的键角为____________,共含有___________个B—B键。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备1,2—二溴乙烷的反应原理如下:
CH3CH2OH![]() CH2=CH2+H2O
CH2=CH2+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。
用少量溴和足量的乙醇制备1,2—二溴乙烷的装置如图所示:

有关数据列表如下:

回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是________;(填正确选项前的字母)
a. 引发反应 b. 加快反应速度
c. 防止乙醇挥发 d. 减少副产物乙醚生成
(2)在装置C中应加入________,其目的是吸收反应中可能生成的酸性气体;(填正确选项前的字母)
a 水 b 浓硫酸 c 氢氧化钠溶液 d 饱和碳酸氢钠溶液
(3)判断该制备反应已经结束的方法是D装置中____________________________;
(4)将1,2—二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,溶液分层,产物应在______层(填“上”“下”);分离该有机物的方法叫_______________。
(5)若产物中有少量乙醚生成,最好用__________除去;(填正确选项前的字母)
a蒸发 b 蒸馏 c 重结晶
(6)反应过程中应用冷水冷却装置D,其主要目的是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉煤灰是燃煤产生的重要污染物,主要成分有Al2O3、Fe2O3、Fe3O4和SiO2等物质。综合利用粉煤灰不仅能够防止环境污染,还能获得纳米Fe2O3等重要物质。
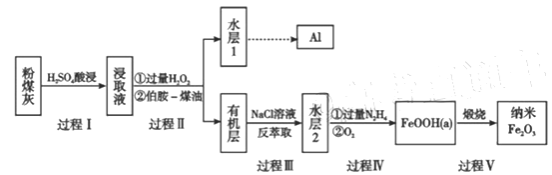
已知:
i)伯胺R-NH2能与Fe3+反应;3R-NH2+Fe3++SO42-+H2O![]() Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
Fe(NH2-R)3(OH)SO4+H+生成易溶于煤油的产物。
ii)Fe3+在水溶液中能与Cl-反应:Fe3++6Cl-![]() [FeCl6]3-,回答下列问题:
[FeCl6]3-,回答下列问题:
(1)过程I对煤粉灰进行酸浸过滤后,滤渣的主要成分是_________。
(2)写出过程II加入过量H2O2发生的离子方程式_________。加入伯胺-煤油对浸取液进行分离,该操作的名称是_________。
(3)从化学平衡角度解释过程III利用NaCl溶液进行反萃取的原理________。
(4)过程IV中过量的N2H4将水层2中[FeCl6]3-转化为Fe2+,得到的Fe2+再被O2氧化为FeOOH,其中第一步的离子方程式为4[FeCl6]3-+5N2H4=4Fe2++N2+.4N2H5++24Cl-,该反应中氧化剂与还原剂的物质的量之比为_________。
(5)在常压用纳米Fe2O3电化学法合成氨的装置如图所示。
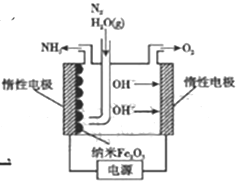
已知电解液为熔融NaOH-KOH,纳米Fe2O3在阴极发生电极反应分两步进行:该电解池第二步:2Fe+N2+3H2O=Fe2O3+2NH3。则该电解池第一步发生反应的方程式为_________。纳米Fe2O3在电解过程中所起的作用是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 电解饱和MgCl2溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
B. 向酸性KMnO4溶液中通入SO2:3SO2+2MnO4-+4OH-===2MnO2↓+3SO42-+2H2O
C. 向Fe(NO3)2稀溶液中滴加足量氢碘酸:3Fe2++NO3-+4H+===3Fe3++NO↑+2H2O
D. 向NaClO溶液中通入足量CO2:ClO-+CO2+H2O===HClO+HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在120℃时,某混合烃和过量O2在一密闭容器中完全反应,测知反应前后的压强没有变化,则该混合烃可能是
A.CH4和C2H4B.C2H2和C2H4C.C2H4和C2H6D.C3H4和C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.
(1)氢气在O2中燃烧的反应是______热反应(填“放”或“吸”),这是由于反应物的总能量______生成物的总能量(填“大于”、“小于”或“等于”,下同);
(2)从化学反应的本质角度来看,氢气的燃烧是由于断裂反应物中的化学键吸收的总能量______形成产物的化学键放出的总能量。已知破坏1mol H-H键、1mol O=O键、1mol H-O键时分别需要吸收a kJ、b kJ、c kJ的能量。则2mol H2(g)和1mol O2(g)转化为2mol H2O(g)时放出的热量为
____________________kJ。
(3)通过氢气的燃烧反应,可以把氢气中蕴含的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中蕴含的化学能转化为电能,下图就是能够实现该转化的装置(其中电解质溶液为KOH溶液),被称为氢氧燃料电池.该电池的正极是___(填a或b),负极反应式为______________。
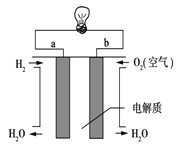
(4)若将右图中的氢氧燃料电池用固体金属氧化物陶瓷作电解质(能够传导O2-),已知正极上发生的电极反应式为:O2+4e-===2O2-则负极上发生的电极反应式为________;电子从________极(填a或b)流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1 mol·L-1某一元酸(HA)溶液中c(OH-)/c(H+)=1×10-8下列叙述正确的是
A. 该一元酸的电离方程式为HA = H++ A-
B. 该溶液中由水电离出的c(H+)=1×10-11mol·L-1
C. 该溶液中水的离子积常数为1×10-22
D. 将pH=11的NaOH溶液V1L与V2L 0.1 mol·L-1该一元酸(HA)溶液混合,若混合溶液的pH=7,则混合溶液中有关离子浓度为c(Na+)>c(OH-)>c(A-)>c(H+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com