
����Ŀ����Դ���ִ�������ԭ������ͨ����ѧ��������ʹ��������������������ʽת�����Ӷ���������Դ�������Դ�������ʣ�
��1��������O2��ȼ�յķ�Ӧ��______�ȷ�Ӧ����š������������������ڷ�Ӧ���������______�������������������ڡ�����С�ڡ����ڡ�����ͬ����
��2���ӻ�ѧ��Ӧ�ı��ʽǶ�������������ȼ�������ڶ��ѷ�Ӧ���еĻ�ѧ�����յ�������______�γɲ���Ļ�ѧ���ų�������������֪�ƻ�1mol H-H����1mol O=O����1mol H-O��ʱ�ֱ���Ҫ����a kJ��b kJ��c kJ����������2mol H2��g����1mol O2��g��ת��Ϊ2mol H2O��g��ʱ�ų�������Ϊ
____________________kJ��
��3��ͨ��������ȼ�շ�Ӧ�������������̺��Ļ�ѧ��ת��Ϊ���ܣ��������������ԭ��Ӧ��Ƴ�ԭ���װ�ã��Ϳ����������̺��Ļ�ѧ��ת��Ϊ���ܣ���ͼ�����ܹ�ʵ�ָ�ת����װ�ã����е������ҺΪKOH��Һ��������Ϊ����ȼ�ϵ�أ��õ�ص�������___����a��b����������ӦʽΪ______________��
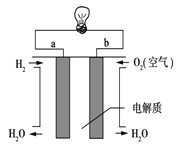
(4)������ͼ�е�����ȼ�ϵ���ù�������������մ�������ʣ��ܹ�����O2��������֪�����Ϸ����ĵ缫��ӦʽΪ��O2��4e��===2O2�����Ϸ����ĵ缫��ӦʽΪ________�����Ӵ�________��(��a��b)������
���𰸡� �� ���� С�� (4c��2a��b)KJ b H2 ��2e-+ 2 OH- = 2H2O 2H2��2O2����4e��===2H2O a
��������(1)ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ������������ȼ�շ�Ӧ�Ƿ��ȷ�Ӧ�����������غ㶨�ɣ����ȷ�Ӧ�Ƿ�Ӧ�����������������������������ʴ�Ϊ���ţ����ڣ�
(2)��ѧ��Ӧ�ı����Ǿɻ�ѧ���Ķ��Ѻ��»�ѧ�����γɣ����ȷ�Ӧ�ı����Ƕ��ѷ�Ӧ���еĻ�ѧ�����յ�������С���γɲ���Ļ�ѧ���ų�����������
�ʱ���ڷ�Ӧ��ļ���֮�ͼ�ȥ������ļ���֮�ͣ���2molH2(g)��1molO2(g)ת��Ϊ2molH2O(g)ʱ�ġ�H=(2��a+b-4��c)kJ��0����ų�������Ϊ(4c��2a��b)KJ���ʴ�Ϊ��С�ڣ�(4c��2a��b)KJ��
(3)����ԭ��ص缫��Ӧ��������ʧ���ӣ�����������Ӧ���������õ��ӣ���Ӧ��ԭ��Ӧ����������ȼ�ϵ�أ�������������Ӧ��ʧ�������������ӣ���ӦΪH2+2e-+2OH-=2H2O���ʴ�Ϊ��b�缫��H2+2e-+2OH-=2H2O��
(4)����ȼ�ϵ�����ù�������������մ�������ʣ������ڸ���ʧȥ���ӷ���������Ӧ���缫����ʽΪ��2H2+2O2--4e-�T2H2O�����ӴӸ�������������a���������ʴ�Ϊ��2H2+2O2--4e-�T2H2O��a��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л��������в�ͬ�ķ����������˵����ȷ����
�������Ԫ�ط֣��������������� ���ӷ�����̼�Ǽ���״�֣���״�л��������״�л������� ���ӹ����ŷ֣�ϩ����Ȳ������������±�����������ӡ�ȩ��ͪ�����ᡢ����
A. �٢� B. �٢� C. �٢ڢ� D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijˮ��Һ�����ܺ��������������������֣�K����NH4+��Cl����Mg2����Ba2����CO32����SO42������ȡ����100 mL��Һ��������ʵ�飺
�ٵ�һ�ݼ�����NaOH��Һ���Ⱥ��ռ�������0.05 mol��
�ڵڶ��ݼ�����BaCl2��Һ�ø������4.3 g������������ϴ�ӡ������������Ϊ2.33 g������˵����ȷ����
A. K��һ������
B. ��Һ��c(Cl��)����Ϊ0.2 mol/L
C. Cl�����ܴ���
D. Ba2��һ�������ڣ�Mg2�����ܴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȫ��ʡ������.������ʡ���н���������2017������߿�ģ�����⣨һ��������˵����ȷ����
A. KAl(SO4)2��Һ�� c(K+)= 2c(SO42-)
B. ��NaHCO3��Һ�м������� Ba(OH)2���壬c(CO32-)����
C. ����AgCl��AgBr���������Һ�У�C(Ag+)>c(Cl-) =c(Br-)
D. �����£���0.1molCH3COOH����Һ�м���amolNaOH���壬��Ӧ����Һ��c(CH3COOH) =c(CH3COO-)������Һ�Լ��ԡ�����֪����Ka =1.75��10-5 )
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����������÷�Һ©���ֿ����ǣ������Ȼ�̼��ˮ ���Ҵ������� �� �Ҵ���ˮ ������ˮ �����顢ˮ �������顢�� ���屽��ˮ
A���ڢۢ� B���٢ڢ� C���٢ܢݢ� D���ܢݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ֱ���������и���Һһ��ʱ�����Һ����ɫ���ܶȱ��ֲ������
A. ��ͭ�缫���ϡH2SO4 B. ��ʯī�缫���Na2SO4��Һ
C. ��ͭ�缫���CuCl2��Һ D. ��Ϊ������пΪ���������ZnCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(2014���������ۣ�11��6��)�����£����й�ϵ��ȷ����( )
A��Na2S��Һ��c(Na��)>c(HS��)>c(OH��)>c(H2S)
B��Na2C2O4��Һ��c(OH��)��c(H��)��c(HC2O![]() )��2c(H2C2O4)
)��2c(H2C2O4)
C��Na2CO3��Һ��c(Na��)��c(H��)��2c(CO![]() )��c(OH��)
)��c(OH��)
D��CH3COONa��CaCl2�����Һ��c(Na��)��c(Ca2��)��c(CH3COO��)��c(CH3COOH)��2c(Cl��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���������ڹ̶������н��еĿ��淴Ӧ2M(g)+N(g)![]() Q(g) ��H>0���ﵽƽ��״̬���������¶ȣ�����ڸû����������˵����ȷ����( )
Q(g) ��H>0���ﵽƽ��״̬���������¶ȣ�����ڸû����������˵����ȷ����( )
A���ܶ����� B��ƽ����Է����������� C�ܷ��������� D��ƽ�������ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ż�����Ⱦ�ļ��غ����ǻ�����ʶ�ļ�ǿ�����オ��������ܵ������ǵĹ�ע��������PBA (�������オ������߷��Ӳ��ϣ��ĺϳ�·�ߣ�

��֪������A����Է�������Ϊ84���˴Ź���������ʾֻ��1��壬����ʹ������Ȼ�̼��Һ��ɫ��
�ڻ�����C��ֻ��һ�������š�
��R1CH=CHR2![]() R1COOH+R2COOH
R1COOH+R2COOH
��
(1)��A����B�ķ�Ӧ����Ϊ_________��
(2)��B����C�Ļ�ѧ����ʽΪ__________��
(3)E�Ľṹ��ʽΪ______________________��
(4)F������Ϊ______________(��ϵͳ������)����D������PBA�Ļ�ѧ����ʽΪ_______________����PBA��ƽ���ۺ϶�Ϊ70������ƽ����Է�������Ϊ___________��
(5)E��ͬ���칹������ͬʱ�������������Ĺ���_____�֣����������칹����
����״������ ���ܷ���������Ӧ ����ԭ�Ӳ���̼̼˫��ֱ������
���У��˴Ź���������ʾΪ2��壬�ҷ������Ϊ2:1����_________(д�ṹ��ʽ)��
(6)����1.3������ϩΪԭ�ϣ��������Լ���ѡ��ͨ�������Ʊ�������F����ϳ�·��Ϊ:___________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com