
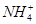 ��Cu2����Ba2����Al3����Ag����Fe3���������ӿ�����Cl����
��Cu2����Ba2����Al3����Ag����Fe3���������ӿ�����Cl���� ��
��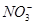 ��
��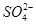 ����֪��
����֪�� ��H2O
��H2O
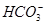 ��OH��
��OH��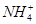
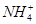 �����õķ����ǽ������ŨNaOH��Һ���ȣ����Ƿ��ܹ�����ʹʪ��ĺ�ɫʯ����ֽ���������塣
�����õķ����ǽ������ŨNaOH��Һ���ȣ����Ƿ��ܹ�����ʹʪ��ĺ�ɫʯ����ֽ���������塣

 53������ϵ�д�
53������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������ƹ�����ˮ��Ӧ��2O22-��2H2O=4OH����O2�� |
| B�����������ڿ�����������4Fe2����3O2��6H2O=4Fe(OH)3�� |
| C�����Ȼ�����Һ�м��������ˮ��Al3����4OH��=AlO2-��2H2O |
| D��̼����þ��Һ�м���������NaOH��Һ��Mg2����2HCO3-��4OH��=Mg(OH)2����2CO32-��2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��NH4����NO3����CO32����Na+ | B��Na+��Ba2+��HCO3����AlO2�� |
| C��NO3����K+��AlO2����OH- | D��NO3����Mg 2+��K+��CH3COO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��Na����Ba2����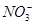 �� ��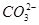 |
B��Ba2����K����Cl����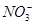 |
C��Mg2����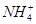 �� ��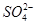 ��Cl�� ��Cl�� |
D��Fe2����Na����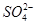 �� ��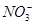 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A����c(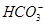 )��0.1 mol��L��1����Һ�У� )��0.1 mol��L��1����Һ�У�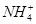 ��Al3����Cl���� ��Al3����Cl����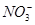 |
B���д���NO���ڵ�ǿ������Һ�У�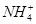 ��Ba2����Fe3����Cl�� ��Ba2����Fe3����Cl�� |
| C����ˮ�������c(H��)��1��10��12mol��L��1����Һ�У�Na����Al3����CH3COO����I�� |
| D����ʹpH��ֽ������Һ�У�ClO����S2����Na����K�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
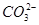 ��
��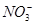 ��
��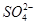 ��
��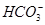 ��
��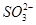 �е����������ӡ�ijͬѧ�Ը���Һ��������ʵ�飺
�е����������ӡ�ijͬѧ�Ը���Һ��������ʵ�飺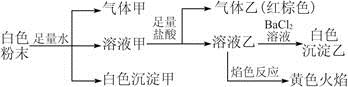
A����ɫ��������Al(OH)3���������CO2�����Ի����һ����Al3����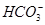 |
| B��������һ����NO��NO2�Ļ������ |
C����ɫ��������BaSO4������ԭ�����һ������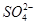 |
| D����ɫ��ӦΪ��ɫ���棬����ȷ��ԭ������в���K�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A������ͬ�¶��£�ͬŨ�ȵ���������Һ�ĵ�������˳�� HZ��HY�� HX |
| B����HZ�м���NaOH��ǡ����ȫ��Ӧʱ,��Һ�и�����Ũ�ȴ�С˳�� c(Na+)��c(Z-)��c(OH��)��c(H+) |
| C��������HX��HY��Һ�������Ϻ���NaOH��Һ�ζ���HXǡ����ȫ��Ӧʱ��c(X��)+c(Y��)+c(OH��)= c(Na+)+c(H+) |
| D����HX��HZ��Һ��Ϻ���NaOH��Һ�ζ���HXǡ����ȫ��Ӧʱ��c(Na+)= c(X��)+ c(Z��) |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ڢ� | C���ڢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com