
【题目】利用电化学原理还原CO2制取ZnC2O4的装置如图所示,下列说法正确的是
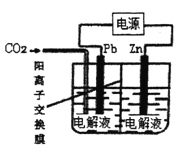
A. Zn电极是阴极
B. C2O42-从左向右移动
C. Pb电极的电极反应式是2CO2-2e-=C2O42-
D. 工作电路中每流过0.02mol电子,Zn电极质量减重0.65g
【答案】D
【解析】
Zn在阳极上失电子生成锌离子,即Zn-2e-=Zn2+,Pb电极上CO2得电子生成C2O42-,即2CO2+2e-=C2O42-,金属锌可以和硫酸之间发生反应,离子交换膜允许部分离子通过,根据电极反应式结合电子守恒来回答。
A.金属Zn失去电子生成ZnC2O4,发生氧化反应,因此Zn连接电源的正极,作阳极,A错误;
B.C2O42-带负电荷,不能通过阳离子交换膜,因此不能从左向右移动,B错误;
C. Pb电极上CO2得电子生成C2O42-,即2CO2+2e-=C2O42-,C错误;
D.Zn在阳极上失电子生成锌离子,即Zn-2e-=Zn2+,每反应产生2mol电子,反应消耗1molZn,溶解的金属Zn的质量是65g,若工作电路中每流过0.02 mol电子,Zn电极质量减重0.65g,D正确;
故合理选项是D。


科目:高中化学 来源: 题型:
【题目】下列关于反应过程中能量变化的说法正确的是

A. 图中a、b曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g) ΔH<0使用和未使用催化剂时,反应过程中的能量变化
B. 己知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2。则ΔH1>ΔH2
C. 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH不同
D. 在一定条件下,某可逆反应的ΔH=+100kJ·mol-1,则该反应正反应活化能比逆反应活化能大100kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用如图所示做水果电池的实验,测得数据如下表所示:
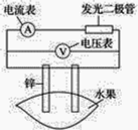
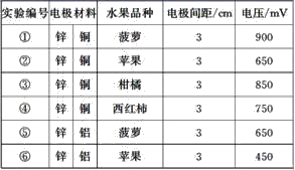
请回答以下问题:
(1)实验⑥中负极的电极反应式为_____________。
(2)实验①、⑤中电流方向相反的原因是_________。
(3)若在实验中发光二极管不亮,该同学用铜、锌作电极,用菠萝作介质,并将多个此电池串联起来,再接发光二极管,这样做________(填“合理”或“不合理”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各实验装置图的叙述中正确的是
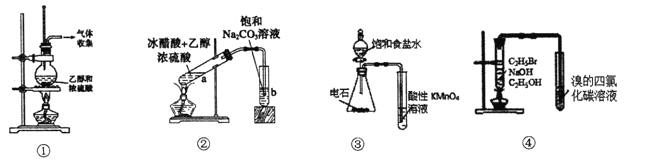
A. 装置①:实验室制取乙烯
B. 装置②:实验室制取乙酸乙酯
C. 装置③:验证乙炔的还原性
D. 装置④:验证溴乙烷发生消去反应可生成烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如右图所示。若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是

A. 原子半径:W>Z>Y>X
B. 最高价氧化物对应水化物的酸性: Z>W>X
C. 4种元素的单质中,Z单质的熔、沸点最高
D. W单质能与水反应,生成一种具有漂白性的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)书写下列物质电子式
①NaOH:_______;②CO2:______;③H2O2:_____;
(2)用电子式表示下列物质的形成过程
①MgCl2:________;
②H2O:__________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由烃A制备抗结肠炎药物H的一种合成路线如下(部分反应略去试剂和条件):
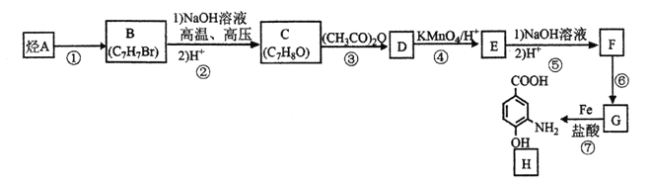
已知:①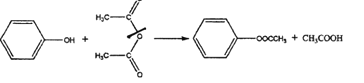
②![]()
请回答下列问题:
(1)H的分子式是___。反应①的试剂和反应条件是___。反应③的类型是__。
(2)E的结构简式是_____。
(3)写出B到C第一步反应的化学方程式是_____。
(4)设计C→D和E→F两步反应的共同目的是____。
(5)F的同分异构体中能同时满足下列条件的共有____种(不含立体异构):①遇FeCl3溶液显紫色,②能发生银镜反应;其中核磁共振氢谱为4组峰的是____(写出其中一种的结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能存在Br-、CO![]() 、SO
、SO![]() 、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
已知:5Cl2+I2+6H2O===10HCl+2HIO3
据此可以判断:该溶液肯定不存在的离子组是
A. Al3+、Mg2+、SO![]() B. Mg2+、CO
B. Mg2+、CO![]() 、I-
、I-
C. Al3+、SO![]() 、I- D. Al3+、Br-、SO
、I- D. Al3+、Br-、SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把22.4g铁粉完全溶解于某浓度的硝酸中,如反应只收集到0.3 mol NO2和0.2 mol NO,下列说法正确的是
A. 反应后生成的盐只为Fe(NO3)3
B. 反应后生成的盐只为Fe(NO3)2
C. 反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为1∶3
D. 反应后生成的盐为Fe(NO3)3和Fe(NO3)2,其物质的量之比为3∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com