
【题目】厌氧氨化法是一种新型的氨氮去除技术,下列说法中正确的是( )
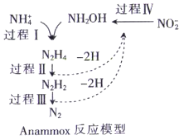
A.1molNH4+中所含的质子总数为10NA
B.1mol联氨(N2H4)中含有5mol共用电子对
C.NH2OH中既含有极性键也含有非极性键
D.该方法每处理1molNH4+,需要的NO2-为0.5mol
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】磁性材料A由两种元素组成,为探究其组成和性质,设计并完成如下实验:
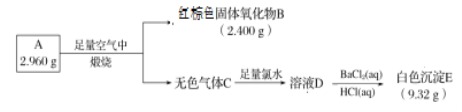
(1) A的化学式为______。
(2) 用化学方程式表达气体C与氯水反应生成D的过程:________。
(3) B溶于盐酸后生成的物质F可用于净水,其原因是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯是一种重要的化工原料,苯可以进行如下转化。部分反应条件、反应物、生成物已省略

(1)反应①的化学方程式是________。
(2)A的结构简式是________名称是________。
(3)反应③所需反应物除A外,还需要________,反应条件是________。
(4)仅用水鉴别苯和溴苯的方法是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早期发现的一种天然二十面体准晶颗粒由Al、Ca、Cu、Fe 四种金属元素组成,回答下列问题:
(1)基态 Fe原子有________个未成对电子,Fe3+的价电子排布式为________。
(2)新制的Cu(OH)2可将乙醛氧化成乙酸,而自身还原成Cu2O。乙醛分子中含有的σ键与π键的比值为_____。乙醛中碳原子的杂化轨道类型为____,配合物[Cu(NH3)4](OH)2中含有的化学键类型有_____。
(3)Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有____个铜原子;金属铜采取如图甲所示堆积方式,可称为_____堆积。。
(4)CaCl2熔点高于AlCl3的原因________。
(5)CaF2晶胞如图乙所示,已知:氟化钙晶体密度为ρg·cm-3 , NA代表阿伏加德罗常数的值。氟化钙晶体中Ca2+和F-之间最近核间距(d)为________cm(只要求列出计算式即可)。
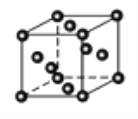 (甲)
(甲) 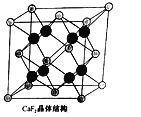 (乙)
(乙)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)某学生为了探究锌与盐酸反应过程中的速率变化,在200mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(累计值):
时间(min) | 1 | 2 | 3 | 4 | 5 |
氢气体积(mL)(标准状况) | 50 | 120 | 232 | 290 | 310 |
①上述实验过程中,反应速率最大时间段是________(选填字母作答),该时间段反应速率最大的主要原因是________________________________________________________。
A.0~1min B.1~2min C.2~3min D.3~4min E.4~5min
②求2~3分钟时间段以盐酸的浓度变化来表示的该反应速率___________________(假设反应过程中溶液体积不变)。
(2)某温度下在容积为1L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是______________________________________________。
②该反应达到平衡状态的标志是________。
A.X的浓度不再改变
B.Y的体积分数在混合气体中保持不变
C.容器内气体的总压强保持不变
D.容器内气体的总质量保持不变
③反应进行到2min时,Y的转化率为_____________。
(3)燃料电池可以将气体燃料和氧气直接反应产生电能,其效率高、污染低,是一种很有前途的能源利用方式。但传统燃料电池使用氢气为燃料,而氢气既不易制取又难以储存,导致燃料电池成本居高不下。科研人员尝试用便宜的甲烷、乙烷等碳氢化合物为燃料,设计出新型燃料电池,使其成本大大低于以氢气为燃料的传统燃料电池。请写出以甲烷为燃料、硫酸为电解质溶液的该新型燃料电池工作时负极的电极反应方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 恒容密闭容器中进行的反应:A(s)+3B(g)![]() 2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
C. N2(g) + 3H2(g)![]() 2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
D. A(g)+ 3B (g) ![]() 2C (g) + D (g),在两种不同情况下的反应速率分别为:①
2C (g) + D (g),在两种不同情况下的反应速率分别为:①![]() ,②
,②![]() ,则前者比后者快
,则前者比后者快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2的捕捉、封存与再利用是实现温室气体减排的重要途径之一。请回答:
(1)二氧化碳的电子式为__________。
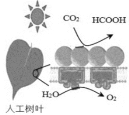
(2)一种正在开发的利用二氧化碳制取甲酸(HCOOH)的途径如图所示,图中能量主要转化方式为_____________ ,CO2和H2O转化为甲酸的化学方程式为____________。
(3)目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g)。
①恒容容器中,能加快该反应速率的是_______。
a.升高温度 b.从体系中分离出CH3OH c.加入高效催化剂 d.降低压强
②在体积为2L的密闭容器中,充入1molCO2和3molH2,测得CO2的物质的量随时间变化如图所示。从反应开始到5min末,用H2浓度变化表示的平均反应速率________________。
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
③在相同温度、恒容的条件下,能说明该反应已达平衡状态的是_______(填序号)。
a.CO2、H2、CH3OH、H2O的浓度均不再改变化
b.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
c.容器中混合气体的密度不变
d.v消耗(H2)=3v消耗(CH3OH)
e.体系压强不变
(4)下列一些共价键的键能如下表所示:
化学键 | H-H | H-O | C=O | C-H | C-O |
键能kJ/mol | 436 | 463 | 803 | 414 | 326 |
反应CO2(g)+3H2(g)CH3OH(g)+H2O(g),______(填“吸收”或“放出”) 的热量为_____kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用图示装置进行实验,不能得出相应结论的是( )
溶液① | 固体② | 溶液③ | 实验结论 |
| |
A | 稀硫酸 | Na2CO3 | Na2SiO3 | 非金属性:S>C>Si | |
B | 浓盐酸 | KMnO4 | Na2S | 氧化性:KMnO4>Cl2>S | |
C | 浓H2SO4 | Cu | 氢硫酸 | 溶液变浑浊 | |
D | 浓氨水 | CaO | AlCl3 | 可以制备Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】R、W、X、Y、M是原子序数依次增大的五种主族元素。R最常见同位素的原子核中不含中子。W与X可形成两种稳定的化合物:WX和WX2。工业革命以来,人类使用的化石燃料在燃烧过程中将大量WX2排入大气,在一定程度导致地球表面平均温度升高。Y与X是同一主族的元素,且在元素周期表中与X相邻。
(1)W的原子结构示意图是__________________________。
(2)WX2的电子式是_______________________。
(3)R2X、R2Y中,稳定性较高的是____(填化学式),请从原子结构的角度解释其原因:_____。
(4)Se与Y是同一主族的元素,且在元素周期表中与Y相邻。
①根据元素周期律,下列推断正确的是________(填字母序号)。
a.Se的最高正化合价为+7价
b.H2Se的还原性比H2Y强
c.H2SeO3的酸性比H2YO4强
d.SeO2在一定条件下可与NaOH溶液反应
②室温下向SeO2固体表面吹入NH3,可得到两种单质和H2O,该反应的化学方程式为_____________。
(5)科研人员从矿石中分离出一种氧化物,化学式可表示为M2O3。为确定M元素的种类,进行了一系列实验,结果如下:
①M的相对原子质量介于K和Rb(铷)之间;
②0.01 mol M2O3在碱性溶液中与Zn充分反应可得到M的简单氢化物,反应完全时,被M2O3氧化的Zn为0.06 mol;
综合以上信息推断,M可能位于元素周期表第_________________族。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com