
 CH3OH(g)+Q
CH3OH(g)+Q | A������CH3OH������������CO��������� | B�����������ܶȲ��� |
| C����������ƽ����Է����������� | D��CH3OH��CO��H2��Ũ�ȶ����ٷ����仯 |
| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| ���� | X | Y | Z | W |
| ��ʼŨ��/mol��L-1 | 0.5 | 0.6 | 0 | 0 |
| ƽ��Ũ��/mol��L-1 | 0.1 | 0.1 | 0.4 | 0.6 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2CO2��N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��²�ò�ͬʱ���NO��COŨ�����±���
2CO2��N2��Ϊ�˲ⶨ��ij�ִ��������µķ�Ӧ���ʣ���ij�¶��²�ò�ͬʱ���NO��COŨ�����±���| ʱ�䣨s�� | 0 | 2 | 4 |
| c��NO�� �� mol��L��1�� | 1.00��10��3 | 2.50��10��4 | 1.00��10��4 |
| c��CO�� �� mol��L��1�� | 3.60��10��3 | c�� | 2.70��10��3 |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���
2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���| ���� | X | Y | Z |
| ��ʼŨ��/mol��L-1 | 0.1 | 0.2 | 0 |
| 2 minĩŨ��/mol��L-1 | 0.08 | a | b |
| ƽ��Ũ��/mol��L-1 | 0.05 | 0.05 | 0.1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
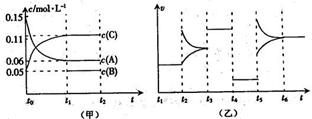
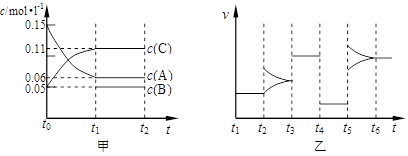
 A����Ӧ�ķ���ʽΪ3A(g)+B(g) 2C(g)
A����Ӧ�ķ���ʽΪ3A(g)+B(g) 2C(g) �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
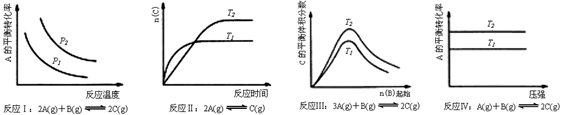
| A����Ӧ��H��0��p2��p1 |
| B����Ӧ��H>0��T1��T2 |
| C����Ӧ��H��0��T2��T1�����H��0��T2��T1 |
| D����Ӧ������H��0��T2��T1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3CH2OH(g)+3H2O(g) ��Q��Q��0��
CH3CH2OH(g)+3H2O(g) ��Q��Q��0��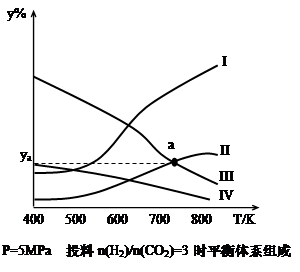
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com