
【题目】下列有机化合物的名称中,正确的是( )
A.2-乙基丁烷B.2,4,5-三氯己烷
C.2,5-二甲基已烷D.2-乙基-2-丁烯
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是
A.CuCl2 [H2O]B.NaOH [NaOH]C.NaCl [Cl2]D.CuSO4 [CuO]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化 钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是 ( )
A. NaOHB. NH3·H2OC. AgNO3D. BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017天津]常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A.增加c(CO),平衡向正向移动,反应的平衡常数增大
B.第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C.第二阶段,Ni(CO)4分解率较低
D.该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2CO(g)+O2(g)![]() 2CO2(g) ΔH=566 kJ·mol1;Na2O2(s)+CO2(g)
2CO2(g) ΔH=566 kJ·mol1;Na2O2(s)+CO2(g)![]() Na2CO3(s)+
Na2CO3(s)+![]() O2(g) ΔH=226 kJ·mol1
O2(g) ΔH=226 kJ·mol1
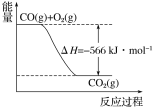
根据以上热化学方程式和图像判断,下列说法正确的是
A.CO的燃烧热为283 kJ
B.上图可表示由1 mol CO生成CO2的反应过程和能量关系
C.2Na2O2(s)+2CO2(s)===2Na2CO3(s)+O2(g) ΔH>452 kJ·mol1
D.根据以上热化学方程式无法求算Na2O2(s)+CO(g)===Na2CO3(s)的反应热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的描述正确的是( )
A. 实验室配制CuCl2溶液时,需加入盐酸来抑制Cu2+水解
B. 定容时仰视容量瓶的刻度线,会导致所配溶液的浓度偏高
C. 用NaOH标准溶液滴定未知浓度的盐酸,未润洗锥形瓶会导致结果偏低
D. 称取2.0gNaOH固体时,先将天平调平,再将游码调至2.0g,向左盘加NaOH固体至天平平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NOx、SO2、CO等大气污染气体的处理具有重要意义。
(1)处理含CO、SO2烟道气污染的一种方法是将其在催化剂作用下转化为单质S。已知:
①CO(g)+![]() O2(g)===CO2(g) ΔH=283.0 kJ·mol1
O2(g)===CO2(g) ΔH=283.0 kJ·mol1
②S(s)+O2(g)===SO2(g) ΔH=296.0 kJ·mol1
此反应的热化学方程式是___________________________________。
(2)氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。已知:
CO(g)+NO2(g)===NO(g)+CO2(g) ΔH=a kJ·mol1(a>0)
2CO(g)+2NO(g)===N2(g)+2CO2(g) ΔH=b kJ·mol1(b>0)
若用标准状况下3.36 L CO还原NO2至N2(CO完全反应)的整个过程中转移电子的物质的量为________mol,放出的热量为______________kJ(用含有a和b的代数式表示)。
(3)用CH4催化还原NOx也可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH1=574 kJ·mol1①
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH2=?②
若1 mol CH4还原NO2至N2,整个过程中放出的热量为867 kJ,则ΔH2=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置就能实现相应实验目的是( )
选项 | 实验目的 | 实验仪器或装置 |
A | 除去KCl中少的 MnO2 | 烧杯、玻璃棒、分液漏斗 |
B | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 100mL容量瓶、玻璃棒、烧杯 |
C | 用氯化钠溶液制备氯化钠晶体 |
|
D | 用右图装置验证SO2的漂白性 |
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com