
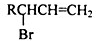
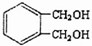
 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式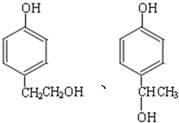 (其中之一);
(其中之一);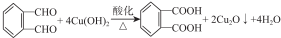 ;
;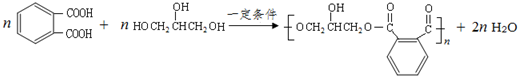 .
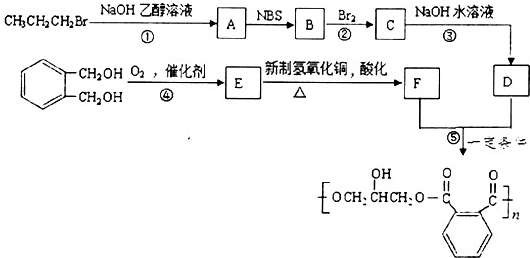
. 分析 CH3CH2CH2Br在氢氧化钠乙醇溶液中发生消去反应生成A为CH3CH=CH2,CH3CH=CH2在NBS作用之下发生取代反应生成B为BrCH2CH=CH2,BrCH2CH=CH2与Br2发生加成反应,生成C为BrCH2CHBrCH2Br,BrCH2CHBrCH2Br再碱性水解发生取代反应生成D为HOCH2CH(OH)CH2OH,根据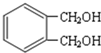 →E→F→
→E→F→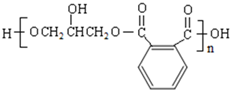 ,结合反应条件可知,E为
,结合反应条件可知,E为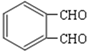 ,F为
,F为 ,据此分析解答.
,据此分析解答.
解答 解:CH3CH2CH2Br在氢氧化钠乙醇溶液中发生消去反应生成A为CH3CH=CH2,CH3CH=CH2在NBS作用之下发生取代反应生成B为BrCH2CH=CH2,BrCH2CH=CH2与Br2发生加成反应,生成C为BrCH2CHBrCH2Br,BrCH2CHBrCH2Br再碱性水解发生取代反应生成D为HOCH2CH(OH)CH2OH,根据 →E→F→
→E→F→ ,结合反应条件可知,E为
,结合反应条件可知,E为 ,F为
,F为 ,
,
(1)B为BrCH2CH=CH2,其官能团名称是溴原子和碳碳双键,故答案为:溴原子和碳碳双键;
(2)反应①、③的有机反应类型分别是消去反应、取代反应或水解反应,故答案为:消去反应;取代反应(或水解反应);
(3)E为 ,含有醛基,能和银氨溶液发生银镜反应、能和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀,故选B、C;
,含有醛基,能和银氨溶液发生银镜反应、能和新制氢氧化铜悬浊液发生氧化反应生成砖红色沉淀,故选B、C;
(4) 的同分异构体中同时符合下列条件:a.能发生消去反应,b.能与过量浓溴水反应生成白色沉淀的芳香族化合物为,说明酚羟基邻位或对位有氢原子,c.苯环上有两个互为对位的取代基,符合条件的结构为
的同分异构体中同时符合下列条件:a.能发生消去反应,b.能与过量浓溴水反应生成白色沉淀的芳香族化合物为,说明酚羟基邻位或对位有氢原子,c.苯环上有两个互为对位的取代基,符合条件的结构为 ,
,
故答案为: (其中之一);
(其中之一);
(5)E发生氧化反应生成F,反应方程式为 ,
,
故答案为: ;
;
(6)反应⑤的化学方程式为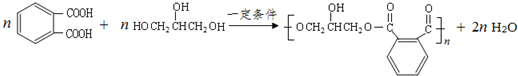 ,
,
故答案为:
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力及知识迁移能力,根据反应条件、物质结构简式结合题给信息进行推断,知道常见反应条件及反应类型的关系,注意(6)题生成水的计量数,为易错点.


科目:高中化学 来源: 题型:选择题
| A. | 硫化橡胶 | B. | 酚醛树脂 | C. | 聚乙烯塑料 | D. | 硝酸纤维 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
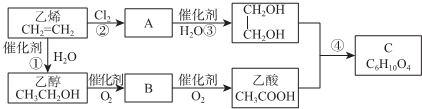
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 实验药品 | 实验器材(省略加持装置) | |
| A | 制备氧气 | 双氧水、二氧化锰 | 分液漏斗、烧瓶、酒精灯、导管 |
| B | 除去CO2中的HCl气体 | 饱和Na2CO3溶液 | 洗气瓶、导管 |
| C | 配制0.5mol/L、230mL的稀硫酸溶液 | 用98%、1.84g/mL的浓硫酸6.8ml | 10mL量筒、烧杯、玻璃棒、胶头滴管、250容量瓶 |
| D | 检验碳与浓硫酸加热产生的气体中是否含有CO2 | 澄清石灰水 | 烧杯、导管 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
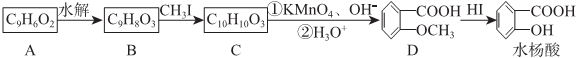
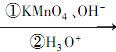 RCOOH+R1COOH
RCOOH+R1COOH .
.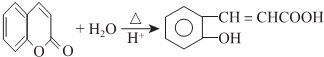 .
.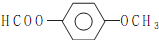 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
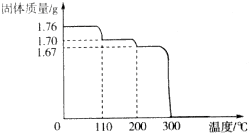

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该锂电池在放电过程中,Li+从正极区向负极区迁移 | |
| B. | 电解质溶液中混入水,对电池反应无影响 | |
| C. | 电池工作过程中,亚硫酰氯(SOCl2)被还原为Li2SO3 | |
| D. | 电池工作过程中,金属锂提供的电子与正极生成硫的物质的量之比为4:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com