
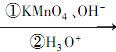 RCOOH+R1COOH
RCOOH+R1COOH .
. .
. .
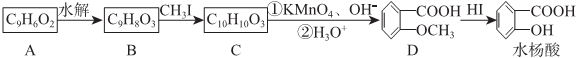
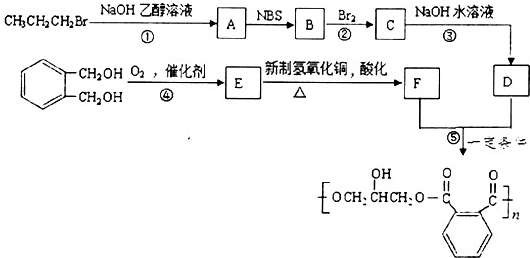
.分析 (1)A反水解反应反应生成B,结合A、B分子式可知A为环状酯类物质,B中含有羧基、羟基,D与HI之间的反应为取代反应;
(2)结合水杨酸的结构简式,可知B的结构简式为 ,再结合B、C、D的转化条件及D的结构简式,可知C为
,再结合B、C、D的转化条件及D的结构简式,可知C为 ,C氧化后另外一种有机物为乙二酸.因苯环上的酚羟基易被氧化,转化为-OCH3,防止被氧化;
,C氧化后另外一种有机物为乙二酸.因苯环上的酚羟基易被氧化,转化为-OCH3,防止被氧化;
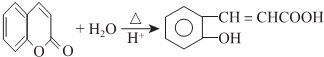
(3)A→B发生酯的水解反应生成 ,A的结构简式为
,A的结构简式为 ;
;
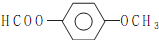
(4)能发生水解反应及银镜反应,说明含有甲酸形成的酯基-OOCH,又是苯的二元取代物,2个取代基为-OOCH、-OCH3,或者为-OOCH、-CH2OH,或者为-CH2OOCH、-OH,各有邻、间、对3种;
(5)ClCH2CH2CH2CH2Cl在氢氧化钠醇溶液、加热条件下发生消去反应生成CH2=CHCH=CH2,然后碱性高锰酸钾溶液氧化,并酸化得到HOOC-COOH.
解答 解:(1)A反水解反应反应生成B,结合A、B分子式可知A为环状酯类物质,B中含有羧基、羟基,D与HI之间的反应为取代反应,
故答案为:羧基、羟基;取代反应;
(2)结合水杨酸的结构简式,可知B的结构简式为 ,再结合B、C、D的转化条件及D的结构简式,可知C为
,再结合B、C、D的转化条件及D的结构简式,可知C为 ,C氧化后另外一种有机物为乙二酸,结构简式为HOOC-COOH.因苯环上的酚羟基易被氧化,转化为-OCH3,保护-OH,避免其被KMnO4溶液氧化,水扬酸可发生聚合反应生成一种高分子化合物,该化合物的结构简式为
,C氧化后另外一种有机物为乙二酸,结构简式为HOOC-COOH.因苯环上的酚羟基易被氧化,转化为-OCH3,保护-OH,避免其被KMnO4溶液氧化,水扬酸可发生聚合反应生成一种高分子化合物,该化合物的结构简式为 ,
,
故答案为:HOOC-COOH;保护-OH,避免其被KMnO4溶液氧化; ;
;
(3)A→B发生酯的水解反应生成 ,A的结构简式为
,A的结构简式为 ,反应方程式为:
,反应方程式为: ,
,
故答案为: ;
;
(4)能发生水解反应及银镜反应,说明含有甲酸形成的酯基-OOCH,又是苯的二元取代物,2个取代基为-OOCH、-OCH3,或者为-OOCH、-CH2OH,或者为-CH2OOCH、-OH,各有邻、间、对3种,共有9种,核磁共振氢谱有4个峰的物质的结构简式为: ,
,
故答案为:9; ;
;
(5)ClCH2CH2CH2CH2Cl在氢氧化钠醇溶液、加热条件下发生消去反应生成CH2=CHCH=CH2,然后碱性高锰酸钾溶液氧化,并酸化得到HOOC-COOH,合成路线流程图为:ClCH2CH2CH2CH2Cl$→_{△}^{氢氧化钠醇溶液}$CH2=CHCH=CH2$→_{ii.H_{3}O+}^{i.KMnO_{4}、OH-}$HOOC-COOH,
故答案为:ClCH2CH2CH2CH2Cl$→_{△}^{氢氧化钠醇溶液}$CH2=CHCH=CH2$→_{ii.H_{3}O+}^{i.KMnO_{4}、OH-}$HOOC-COOH.
点评 本题考查有机物的推断与合成,充分利用有机物分子式、结构简式与反应条件进行分析,较好地考查学生分析推理能力、知识迁移运用能力.


科目:高中化学 来源: 题型:选择题
| A. | 天然蛋白质中仅含C、H、0、N四种元素 | |
| B. | 加入(NH4)2S04饱和溶液会使蛋白质变性 | |
| C. | 重金属盐能使蛋白质凝结,所以误食重金属盐会中毒 | |
| D. | 鸡蛋清加入食盐,会使蛋白质变性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,将1 mol N2和3 mol H2混合发生反应,转移的电子总数为6 NA | |
| B. | 1 L 0.1 mol•L-1的Na2CO3溶液中阴离子的总数大于0.1 NA | |
| C. | 标准状况下,44.8LHF中含有分子的数目为2NA | |
| D. | 1 mol-CH3中所含的电子总数为10 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
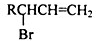
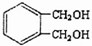 的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式
的同分异构体中同时符合下列条件的芳香族化合物,试写出其中一种的结构简式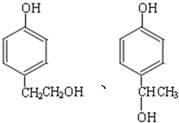 (其中之一);
(其中之一);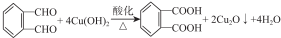 ;
;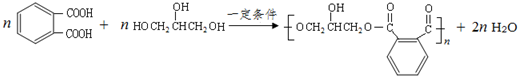 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 装置 | 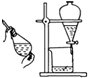 | 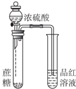 | 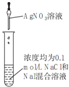 | 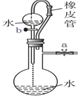 |
| 目的 | 用NaOH溶液除去溴苯中单质溴 | 证明浓硫酸有脱水性、强氧化性 | 确定Ksp(AgCl)、Ksp(AgI)的相对大小 | 观察水能否全部流下判断装置气密性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色的碱性溶液中:CrO42-、K+、Na+、SO42- | |
| B. | 含有大量ClO-的溶液中:K+、H+、I-、SO42 | |
| C. | -使pH试纸变红的溶液中:NH4+、Na+、SO42-、Cl- | |
| D. | 水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 结晶氯化钠 | B. | 金刚石 | C. | 碳酸钙 | D. | 二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
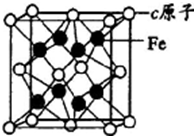 a、b、c、d是四种原子序数依次增大的短周期元素.a原子的电子层数为n,核内质子数是2n2-1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的.回答下列问题:
a、b、c、d是四种原子序数依次增大的短周期元素.a原子的电子层数为n,核内质子数是2n2-1,最外层电子数为2n+l;b、d同主族,能形成两种中学常见的化合物;c与b组成的化合物是一种两性氧化物,工业上通过电解该化合物可冶炼c单质;e原子有四个能层,其未成对电子数在同周期是最多的.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
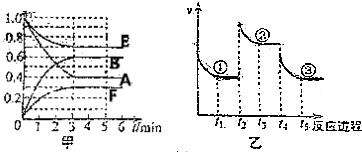
| A. | t2时刻可能是增大压强 | |
| B. | 平衡状态①和②,平衡常数K一定相同 | |
| C. | 平衡状态①、②和③中,状态③中F的浓度最大 | |
| D. | t4时刻改变的条件是降低温度 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com