
【题目】二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是___________________
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总数_______
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示


写出沉淀变化由a到b的离子方程式:_________________________________________________________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;
并写出与上图中不同曲线处对应的离子反应方程式__________________________________;
_______________________________________________________________。
【答案】MgO 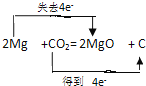 CaCO3 + CO2 + H2O = Ca2+ + 2HCO3-
CaCO3 + CO2 + H2O = Ca2+ + 2HCO3- 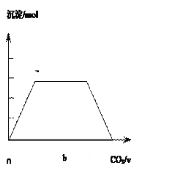 CO2+ 2OH- = CO32- + H2O、CO32-+CO2+ H2O = 2HCO3-
CO2+ 2OH- = CO32- + H2O、CO32-+CO2+ H2O = 2HCO3-
【解析】
I.①Mg在二氧化碳中燃烧生成C和MgO;
②根据元素的化合价变化及电子转移的数目来用“双线桥法”表示反应中电子转移的方向和总数,箭头的起点和终点都指向同种元素;
II.CO2与Ca(OH)2反应生成碳酸钙沉淀,当CO2过量碳酸钙沉淀又溶解生成碳酸氢钙;
III.CO2通入KOH和Ca(OH)2的混合溶液中,CO2先与Ca(OH)2反应生成碳酸钙沉淀,然后再与KOH反应生成碳酸钾,二氧化碳过量时与碳酸钾反应生成碳酸氢钾、与碳酸钙反应生成碳酸氢钙.
Ⅰ.①Mg在二氧化碳中燃烧生成C和MgO,其反应为2Mg+CO2 ![]() 2MgO+C,Mg元素的化合价升高被氧化,则氧化产物为MgO;
2MgO+C,Mg元素的化合价升高被氧化,则氧化产物为MgO;
②2Mg+CO2 ![]() 2MgO+C,C元素的化合价由+4降低为0,得4e-,Mg元素的化合价由0升高到+2,失2×2e-,则用“双线桥法”表示反应中电子转移的方向和总数为
2MgO+C,C元素的化合价由+4降低为0,得4e-,Mg元素的化合价由0升高到+2,失2×2e-,则用“双线桥法”表示反应中电子转移的方向和总数为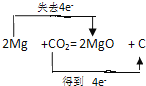 ;
;
II.CO2与Ca(OH)2反应生成碳酸钙沉淀,当CO2过量碳酸钙沉淀又溶解生成碳酸氢钙,根据图中沉淀变化及所用二氧化碳的比例为1:1,由a到b的离子方程式:CaCO3+CO2+H2O=Ca2++2HCO3-;
III.另一份先加入少量的KOH固体溶解,CO2通入KOH和Ca(OH)2的混合溶液,CO2先与Ca(OH)2反应生成碳酸钙沉淀,发生Ca2++CO2+2OH-=CaCO3↓+H2O,生成的碳酸钙沉淀的物质的量与II中相同,然后再与KOH反应生成碳酸钾,离子方程式为:CO2+2OH-=CO32-+H2O,过量的二氧化碳与碳酸钾反应生成碳酸氢钾,此时碳酸钙沉淀的物质的量不变,离子方程式为:CO32-+CO2+H2O=2HCO3-,最后CO2与碳酸钙反应生成碳酸氢钙,发生CaCO3+CO2+H2O=Ca2++2HCO3-,沉淀逐渐溶解,沉淀的物质的量逐渐减少,直到消失,生成沉淀的物质的量(n)和通入CO2体积(V)的关系图为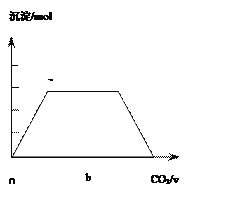 。图中平台部分与原图不同,不同曲线处对应的离子反应方程式:CO2+ 2OH-= CO32-+ H2O 、CO32-+CO2+ H2O = 2HCO3-。
。图中平台部分与原图不同,不同曲线处对应的离子反应方程式:CO2+ 2OH-= CO32-+ H2O 、CO32-+CO2+ H2O = 2HCO3-。


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:
【题目】使用胆矾(CuSO45H2O)配制0.1 molL-1的硫酸铜溶液,正确的操作是( )
A. 将胆矾加热除去结晶水后,称取16g溶解在1 L水中
B. 称取25 g胆矾溶于水,然后将此溶液稀释至1 L
C. 称取25 g胆矾溶解在1 L水里
D. 将16 g胆矾溶于水,然后将此溶液稀释至1 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在如图所示转化关系(部分生成物和反应条件略去);已知A 由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:
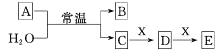
(1)若A为单质,且C为一元强酸。
①化合物B 的结构式为_______。
②写出一种工业制备单质A的离子方程式:________。
③X可能为______(填字母代号)。
a.NaOH b.AlCl3 c.Na2CO3 d.Na[Al(OH)4]
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A的电子式为______。
②A与H2O反应的化学方程式为_____。
③室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如下图所示,下列说法中不正确的是( )
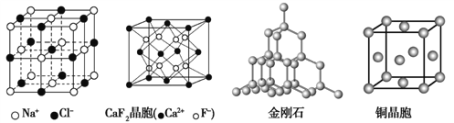
A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子数与碳碳键个数的比为1:4
D. 铜晶体为面心立方最密堆积,该晶体中面对角线长度为原子半径的4倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式C8H8O2.A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图.关于A的下列说法中,正确的是( )
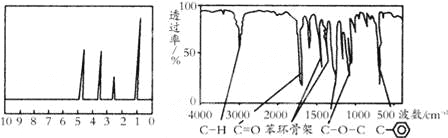
A. A分子属于酯类化合物,在一定条件下能发生水解反应
B. A在一定条件下可与4 mol H2发生加成反应
C. 符合题中A分子结构特征的有机物有两种
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )
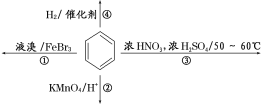
A. 反应①常温下不能进行
B. 反应②不发生,但是仍有分层现象,紫色层在下层
C. 反应③为取代反应,有机产物是一种烃的衍生物
D. 反应④能发生,从而证明苯中是单双键交替结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于太阳能、生物质能和氢能的利用的说法不正确的是![]()
![]()
A. 光伏电池可实现太阳能到电能的转化
B. 将植物的秸秆、枝叶、杂草和人畜粪便加入沼气发酵池中,在富氧条件下,经过缓慢、复杂、充分的氧化反应最终生成沼气,从而有效利用生物质能
C. 生活、生产中大量应用氢能源,要解决氢气的储存和运输等问题
D. 垃圾焚烧处理厂把大量生活垃圾中的生物质能转化为热能、电能,减轻了垃圾给城市造成的压力,改善了城市的环境
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液X中可能含有下列离子中的若干种:Cl-、SO42-、SO32-、HCO3-、Na+、Mg2+、Fe3+,所含离子的物质的量浓度均相同。为了确定该溶液的组成,某同学取100mL上述溶液X,进行了如下实验:(1)向溶液X中加入足量的Ba(OH)2溶液,得到白色沉淀:(2)将(1)的反应混合液过滤,将足量盐酸加入沉淀中,沉淀部分溶解且产生气体。
下列说法正确的是![]()
![]()
A. (2)中产生的气体可能CO2或SO2
B. 溶液X中一定存在SO42-、HCO3-、Mg2+
C. 溶液X中一定不存在Fe3+,可能存在Cl-
D. (1)中产生的白色沉淀一定含有BaSO4,可能含有BaSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)相对分子质量为86的烷烃的分子式是 _________。
(2)用系统命名法命名: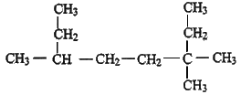 _______________________。
_______________________。
(3)用系统命名法命名: 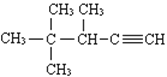 ______________________________。
______________________________。
(4)顺-2-丁烯的结构简式为_________________________。
(5)碳原子数1-10的烷烃中一氯代物只有一种的烷烃有4种,它们的结构简式为CH4、CH3CH3、_____________________、_____________________。
(6)实验室制取乙炔的化学方程式为_______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com