
【题目】A、B、C、D、E、X均为短周期元素形成的无机物,存在如图所示转化关系(部分生成物和反应条件略去);已知A 由短周期非金属元素组成,B具有漂白性且光照易分解。请回答以下问题:
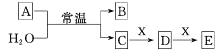
(1)若A为单质,且C为一元强酸。
①化合物B 的结构式为_______。
②写出一种工业制备单质A的离子方程式:________。
③X可能为______(填字母代号)。
a.NaOH b.AlCl3 c.Na2CO3 d.Na[Al(OH)4]
(2)若A为两种元素形成的化合物,且E与水反应生成的G的浓溶液遇C有白烟产生。
①A的电子式为______。
②A与H2O反应的化学方程式为_____。
③室温下,NH2OH(羟氨)会发生分解生成C、D,试写出其分解反应的化学方程式_________。
【答案】H—O—Cl 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑ cd
2OH-+H2↑+Cl2↑ cd 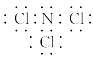 NCl3+3H2O=3HClO+NH3 5NH2OH=3NH3↑+2NO↑+3H2O
NCl3+3H2O=3HClO+NH3 5NH2OH=3NH3↑+2NO↑+3H2O
【解析】
A、B、C、D、E、X均为短周期元素形成的无机物,A由短周期非金属元素组成,B具有漂白性且光照易分解,则B为HClO;
(1)若A为单质,且C为一元强酸,则C为HCl,A为Cl2,X可能为Na2CO3、Na[Al(OH)4]等;
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生,则C为NH3,结合B为HClO,根据元素守恒可及化合价的情况可知A为NCl3,时而推得G为HNO3,E为NO2,X为氧气,符合转化关系,以此解答该题。
A、B、C、D、E、X均为短周期元素形成的无机物,A由短周期非金属元素组成,B具有漂白性且光照易分解,则B为HClO。
(1)若A为单质,C为一元强酸,则C为HCl,A为Cl2;
①化合物B为HClO,结构式为H—O—Cl。
②工业上电解饱和食盐水制备Cl2,工业制备单质A的离子方程式:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑。
2OH-+H2↑+Cl2↑。
③a.若X为NaOH,NaOH与HCl反应生成的NaCl与NaOH不反应,X不可能为NaOH;b.若X为AlCl3,AlCl3与HCl不反应,X不可能为AlCl3,c.若X为Na2CO3,Na2CO3与HCl反应生成CO2,CO2与Na2CO3、H2O反应生成NaHCO3,X可能为Na2CO3;d.若X为Na[Al(OH)4],Na[Al(OH)4]与过量HCl反应生成AlCl3,AlCl3与Na[Al(OH)4]反应生成Al(OH)3,X可能为Na[Al(OH)4];答案选cd。
(2)若A为两种元素形成的化合物,且E与水反应生成G的浓溶液遇C有白烟产生,则C为NH3,结合B为HClO,根据元素守恒定律及化合价的情况可知A为NCl3,推得G为HNO3,D为NO,E为NO2,X为氧气。
①A的电子式为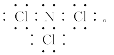
②A与H2O反应的化学方程式为NCl3+3H2O=3HClO+NH3。
③室温下,NH2OH(羟氨)会发生分解生成C、D,其分解反应的化学方程式为5NH2OH=3NH3↑+2NO↑+3H2O。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列实验装置或操作设计正确、且能达到目的的是( )
A. 实验①,设计铜银双液原电池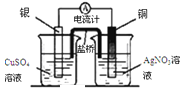
B. 实验②,将钢闸门与外接电源的负极相连,可防止钢闸门腐蚀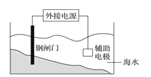
C. 实验③,准确量取一定体积K2Cr2O7标准溶液![]()
D. 实验④,蒸干氯化镁溶液制MgCl2·6H2O 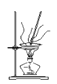
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求答题
(一)现有下列七种物质:①铝 ②蔗糖 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥红褐色的氢氧化铁胶体 ⑦HCl ⑧冰水混合物 ⑨碳酸钙 ⑩CuSO4·5H2O。
(1)上述物质中属于电解质的有__________(填序号)。
(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是________________________。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为______________________________。
(二)(1)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______,R的相对原子质量为__________。
(2)在标准状况下,w L氮气含有x个N2分子,则阿伏加德罗常数为____________(用w,x表示)。
(3)过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图回答问题:如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
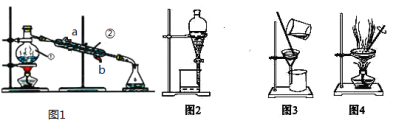
(1)写出上述装置中仪器的名称:①________。
(2)若利用上述装置分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,图1中仪器 ②是从______口进水(填a或b)。
(3)图2在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是______
(4)从氯化钾溶液中得到氯化钾固体,选择装置______(填代表装置图的序号,下同);除去自来水中的Cl等杂质,选择装置______。
(5)实验室常用上述装置分离碘水中的碘,进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。
①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出方程式:实验室制乙炔__________________;
(2)![]() 该有机物共面的原子最多有_____个,与溴发生加成反应的产物最多有_______种
该有机物共面的原子最多有_____个,与溴发生加成反应的产物最多有_______种
(3)有甲、乙两种物质:

由甲转化为乙需经下列过程(已省略去各步反应的无关产物)
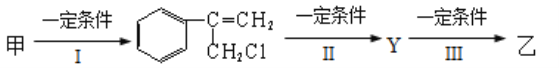
①反应I的反应类型是__________________,
②反应II的条件是_________________________________,
③反应III的化学方程式为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、X、Y、Z是原子序数依次增大的短周期主族元素,Q原子的最外层电子数是内层电子数的2倍,X、Y、Z在周期表中的位置关系如图所示。下列说法正确的是

A. Q和Z可能形成化合物QZ2
B. Y的最高价氧化物的水化物一定是强酸
C. X、Z和氢三种元素不可能组成离子化合物
D. 最简单气态氢化物的沸点:Q>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据科技日报网报道南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现丙烯醇高效、绿色合成。丙烯醇及其化合物可合成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的丙烯醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
(1)基态镍原子的电子排布式为____________________________________________。
(2)1 mol CH2=CH-CH2OH中σ键和π键的个数比为___________,丙烯醇分子中碳原子的杂化类型为___________。
(3)丙醛(CH3CH2CHO的沸点为49℃,丙烯醇(CH2=CHCH2OH)的沸点为91℃,二者相对分子质量相等,沸点相差较大的主要原因是______________________。
(4)羰基镍[Ni(CO)4]用于制备高纯度镍粉,它的熔点为-25℃,沸点为43℃。羰基镍晶体类型是___________。
(5)Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(SCN)3]-和[Ni(CN)4]2-等。[Ni(NH3)6]2+中心原子的配位数是___________ ,与SCN-互为等电子体的分子为___________。
(6)“NiO”晶胞如图所示。

①氧化镍晶胞中原子坐标参数:A(0,0,0)、B(1,1,0),则C原子坐标参数为___________。
②已知:氧化镍晶胞密度为dg/cm3,NA代表阿伏加德罗常数的值,则Ni2+半径为___________nm(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等领域也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳。
Ⅰ.①氧化产物是___________________
②请写出化学反应方程式,并用双线桥法表示该反应的电子转移总数_______
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示


写出沉淀变化由a到b的离子方程式:_________________________________________________________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系;
并写出与上图中不同曲线处对应的离子反应方程式__________________________________;
_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() 的说法中正确的是
的说法中正确的是
A. 所有原子都可能在同一平面上
B. 最多只可能有9个碳原子在同一平面上
C. 有7个碳原子可能在同一直线上
D. 分子中有5个碳原子在同一直线上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com