
| A、食醋用氢氧化钠溶液滴定开始时,溶液的PH通常变化缓慢,当接近完全反应时(即滴定终点),pH出现突变,称为滴定突跃 |
| B、纸层析法分离铁离子和铜离子实验中,点样后的滤纸晾干后将其末端浸入展开剂中约0.5cm |
| C、Cu2+与足量氨水反应的离子方程式 Cu2++2NH3?H2O═Cu(OH)2↓+2NH4+ |
| D、硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 |


科目:高中化学 来源: 题型:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
 )在催化剂作用下发生缩聚反应生成聚乳酸:
)在催化剂作用下发生缩聚反应生成聚乳酸:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)>c(S2-)>c(OH-)>c(HS-) |
| B、c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C、c(Na+)=2c(HS-)+2c(S2-)+2c(H2S) |
| D、c(OH-)=c(H+)+c(HS-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
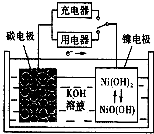 用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
用吸附了氢气的纳米碳管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A、放电时,负极的电极反应为:H2-2e-+2OH-=2H2O |
| B、充电时,阳极的电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O |
| C、放电时,OH-移向镍电极 |
| D、充电时,将电池的碳电极与外电源的正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 阿斯巴甜(Aspartame,结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍.下列有关说法不正确的是( )
阿斯巴甜(Aspartame,结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍.下列有关说法不正确的是( )| A、分子式为:C14H18N2O5,阿斯巴甜属于蛋白质 |
| B、阿斯巴甜能与H2发生加成反应 |
| C、阿斯巴甜在一定条件下既能与酸反应、又能与碱反应 |
| D、阿斯巴甜在一定条件下能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、①③⑤ |
| C、②④⑥ | D、②⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,78 g Na2O2中含有的阴离子数是2NA |
| B、标准状况下,22.4LSO3的物质的量为1mol |
| C、常温常压下,22.4 L SO2和O2混合气体中含有的氧原子数是2 NA |
| D、铁铝混合物与一定量稀盐酸反应生成1 mol H2时,转移电子数是2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com