
 | 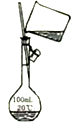 |  | 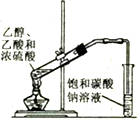 |
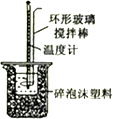
| A测定中和反应的反应热 | B配制100mL0.1mol/L盐酸 | C用来分离乙醇和水 | D实验室制备乙酸乙酯 |
| A、A | B、B | C、C | D、D |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 请根据接触法制硫酸的简单流程图,回答下列问题:
请根据接触法制硫酸的简单流程图,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 可简写为
可简写为 .现有某化合物X的分子结构可表示为
.现有某化合物X的分子结构可表示为 .
.查看答案和解析>>
科目:高中化学 来源: 题型:
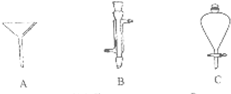 Ⅰ、如图是几种实验中常用的仪器:写出序号所代表的仪器的名称:
Ⅰ、如图是几种实验中常用的仪器:写出序号所代表的仪器的名称:查看答案和解析>>
科目:高中化学 来源: 题型:
A、 |
B、 |
C、 |
D、 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在室温和大气压强下,用如图装置进行实验,测得a g含CaC290%的样品与水完全反应产生的气体体积为 b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:
在室温和大气压强下,用如图装置进行实验,测得a g含CaC290%的样品与水完全反应产生的气体体积为 b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(NH4+)=c(OH-)=c(NH3?H2O) |
| B、c(NH4+)<c(OH-)<c(NH3?H2O) |
| C、c(NH4+)=c(OH-)<c(NH3?H2O) |
| D、c(NH4+)>c(OH-)>c(NH3?H2O) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com