
| A、c(NH4+)=c(OH-)=c(NH3?H2O) |
| B、c(NH4+)<c(OH-)<c(NH3?H2O) |
| C、c(NH4+)=c(OH-)<c(NH3?H2O) |
| D、c(NH4+)>c(OH-)>c(NH3?H2O) |
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
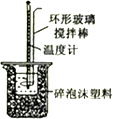 | 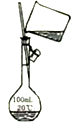 |  | 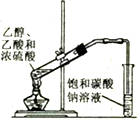 |
| A测定中和反应的反应热 | B配制100mL0.1mol/L盐酸 | C用来分离乙醇和水 | D实验室制备乙酸乙酯 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙酸是实验室常用的化学药品之一.请回答下列问题:
乙酸是实验室常用的化学药品之一.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
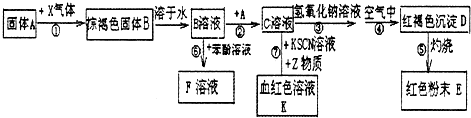
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只有乙醇 |
| B、只有乙酸 |
| C、乙酸乙酯、乙醇、乙酸 |
| D、只有乙醇和乙酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度,平衡向逆反应方向移动,正反应速率减慢 |
| B、容积不变,加入1molN2(N2不参加反应),反应速率不变 |
| C、压强不变,加入1molN2(N2不参加反应),反应速率不变 |
| D、容积不变,加入1molN2,则正反应速率加快,逆反应速率减慢 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com