
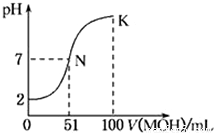
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中,正确的是
A.HA可能为一元弱酸
B.MOH为一元强碱
C.N点水的电离程度小于K点水的电离程度
D.若K点对应的溶液的pH=l0,则有c(MOH)+c(M+)=0.01mol L-1
L-1
D
【解析】
试题分析:A、根据图像可知,开始时0.01mol/L HA溶液中pH=2,这说明溶液中氢离子的浓度是0.01mol/L,因此HA是强酸,A不正确;B、N点时溶液呈中性,消耗MOH的溶液体积是51ml,根据MOH的浓度可知,MOH的物质的量大于HA的物质的量,即MOH过量,但溶液显中性,因此说明MOH是弱碱,B不正确;C、酸或碱溶液抑制水电离,能发生水解的盐促进水电离。N点溶液呈中性,K点MOH过量,溶液显碱性,抑制水的电离,所以N点水的电离程度大于K点水的电离程度,C不正确;D、在K点时混合溶液是MA和MOH的混合液,且二者的浓度相等,所以根据物料守恒结合溶液体积变化知,c(MOH)+c(M+)=0.02mol/L÷2=0.01mol/L,D正确,答案选D。
考点:考查酸碱中和滴定曲线、弱电解质、溶液酸碱性的判断、外界条件对水的电离平衡影响以及溶液中离子浓度关系计算等


科目:高中化学 来源:2012-2013学年山东省威海市高二上学期期末考试化学试卷(带解析) 题型:填空题
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号)。
(2)常温下0.01 mol/L HCl溶液的PH= ;PH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(3)用离子方程式表示CH3COONa溶液呈碱性的原因 ,其溶液中离子浓度按由大到小的顺序为 。
(4)将等PH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的PH仍相等,则m n (填“大于、等于、小于”)。
(5)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题: 
①由图中信息可知HA为_______酸(填“强”或“弱”)。
② K点对应的溶液中,
c(M+)+c(MOH)= mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年山东省德州市高三上学期期末考试化学试卷(解析版) 题型:填空题
I:化学是一门以实验为主的科学,化学实验是学习探究物质性质的基本方法之一。(1)化学实验中,常将溶液或试剂进行酸化,下列酸化处理的措施中正确的是
A.定性检验SO32-,可用HNO3酸化的BaCl2溶液
B.配制FeCl2溶液时通常加少量HNO3酸化,减小其水解程度
C.检验某溶液中是否含Cl-,用HNO3酸化的AgNO3溶液
D.酸性高锰酸钾溶液经常用盐酸酸化
(2)下列有关说法中正确的有??????? ?
①用pH试纸测得氯水的pH为3.5
②用瓷坩埚高温熔融NaOH固体
③加入浓NaOH溶液,加热产生使湿润的红色石蕊试纸变蓝的气体,则原溶液中一定含有NH4+
④向溶液中加入少量双氧水,再加几滴KSCN溶液后溶液变红,则原溶液中一定含有Fe2+
⑤实验时不慎被玻璃划破手指,引起轻微流血时,可用三氯化铁溶液涂抹止血
II:(1)某温度下,纯水中c(H+)=2.0×10-7mol·L-1.该温度下,0.9mol·L-1NaOH溶液与0.1mol·L-1 HCl溶液等体积混合(不考虑溶液体积变化)后,溶液的pH= ???? 。
(2)向含有0.020 molCH3COOH的溶液中加入0.020mol CH3COONa固体,溶液pH增大,主要原因是 ?? ?? ;已知该混合溶液中c(Na+)<c(CH3COO-),则c(CH3COOH)?????? c(CH3COO-)(用“>”、“<”、“=”符号填空)。
(3)常温下,向100 mL 0.01mol·L-1HA溶液逐滴加入0.02mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。

回答下列问题:
①由图中信息可知HA为??? 酸(填“强”或“弱”)。
②K点对应的溶液中,c(M+)+c(MOH)=???? mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2015届甘肃省高二上学期期末考试化学试卷(解析版) 题型:填空题
(1)常温下pH=5 HCl溶液和pH=5的AlCl3溶液中由水电离产生的c (H+) 之比等于 。
(2)写出泡沫灭火器灭火时发生反应的离子方程式 。
(3)常温下将0.01molCH3COONa和0.02mol盐酸溶于水,配成0.5L混合溶液。溶液中共有 种微粒,各离子浓度从大到小的顺序为 。
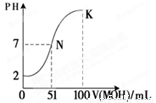
(4)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(忽略溶液混合时的体积变化)。
回答下列问题:
①由图中信息可知HA为_______酸(填“强”或“弱”) ② K点对应的溶液中c(M+)+c(MOH)= mol·L-1。
查看答案和解析>>
科目:高中化学 来源:2014届山东省威海市高二上学期期末考试化学试卷(解析版) 题型:填空题
下列化合物:①HCl ②NaOH ③CH3COOH ④NH3·H2O ⑤CH3COONa ⑥NH4Cl
(1)属于弱电解质的是 ,溶液呈碱性的有 (填序号)。
(2)常温下0.01 mol/L HCl溶液的PH= ;PH=11的CH3COONa溶液中由水电离产生的c(OH-) = 。
(3)用离子方程式表示CH3COONa溶液呈碱性的原因 ,其溶液中离子浓度按由大到小的顺序为 。
(4)将等PH等体积的HCl和CH3COOH分别稀释m倍和n倍,稀释后两溶液的PH仍相等,则m n (填“大于、等于、小于”)。
(5)常温下,向100 mL 0.01 mol·L-1HA溶液逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。回答下列问题:

①由图中信息可知HA为_______酸(填“强”或“弱”)。
② K点对应的溶液中,
c(M+)+c(MOH)= mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com