
【题目】中科院董绍俊课题组将二氧化锰和生物质置于一个由滤纸制成的折纸通道内形成电池(如下图所示),该电池可将可乐(pH=2.5)中的葡萄糖作为燃料获得能量。下列说法正确的是

A. a极为正极
B. 随着反应不断进行,负极区的pH不断增大
C. 消耗0.01mol葡萄糖,电路中转移0.02mol电子
D. b极的电极反应式为:MnO2+2H2O+2e-=Mn2++4OH-
【答案】C
【解析】
此装置为新型电池,为原电池原理,其中a极葡萄糖(C6H12O6)转化为葡糖糖内酯(C6H10O6),C元素化合价升高,发生氧化反应,因电解质的pH=2.5,则为其电极反应式为:C6H12O6 - 2e-= C6H10O6 + 2H+,b极为电源的正极,MnO2失电子发生还原反应,电极反应式为:MnO2+ 4H++2e-=Mn2++2H2O,据此分析作答。
A. 由已知图示可知,葡萄糖(C6H12O6)发生氧化反应生成葡糖糖内酯(C6H10O6),则a极为负极,故A项错误;
B. 由上述分析可知,负极反应式为:C6H12O6 - 2e-= C6H10O6 + 2H+,因此随着反应不断进行,负极区的氰离子浓度逐渐增大,其溶液的pH不断减小,故B项错误;
C. 因负极发生的反应为:C6H12O6 - 2e-= C6H10O6 + 2H+,则消耗0.01 mol葡萄糖,电路中转移0.02 mol电子,故C项正确;
D.因电解质的环境为酸性,则b极的电极反应式为:MnO2+ 4H++2e-=Mn2++2H2O,故D项错误;
答案选C。


 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
【题目】如图所示为元素周期表的一部分,下列有关短周期元素X、Y、Z、W的说法中,正确的是( )
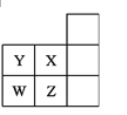
A. 元素X的最低化合价的绝对值与其最高化合价之和为8
B. 最高价氧化物对应的水化物的酸性:H2WO4>HZO4
C. 气态氢化物的稳定性:H2Y>H2W
D. 原子半径:Z>W>Y>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 稳定性:HCl<HBr
B. 氯化钠和冰熔化时,化学键都被破坏
C. H2O2是既含极性键又含非极性键的共价化合物
D. NaOH、NH4Cl、H2SO4在水中均能电离出离子,它们都是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组利用下列装置探究氯气与氨气的反应.其中A、B分别为氯气和氨气的发生装置,C为纯净干燥的氯气与氨气反应的装置.

(1)若Cl2从左向右流动,NH3从右向左流动,则上述实验装置中,依次连接的合理顺序为:A→________________→B;为使NH3与Cl2更充分混合,Cl2应从C装置的__口进入(填“x”或“y”).
(2)简述装置A中使用分液漏斗向圆底烧瓶中滴加浓盐酸的操作是__________________.
(3)装置A中发生反应的离子方程式为_______________________________.
(4)装置B中圆底烧瓶内的试剂为______________(填名称).
(5)装置D的作用是____________________________.
(6)反应开始后,装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气中的主要成分之一,该反应的化学方程式为________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )

A. 若A是铁,则E可能为稀硝酸
B. 若A是CuO,E是碳,则B为CO
C. 若A是NaOH溶液,E是CO2,则B为NaHCO3
D. 若A是AlCl3溶液,E可能是氨水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质之间的转化在给定条件下能实现的是
①S![]() SO2
SO2![]() BaSO4
BaSO4
②CuSO4(aq)![]() Cu(OH)2悬浊液
Cu(OH)2悬浊液![]() Cu2O
Cu2O
③饱和NaCl(aq)![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
④Fe2O3![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
A. ①③ B. ②③ C. ②④ D. ①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 钠与水反应:Na+2H2O═Na++2OH﹣+H2↑
B. 电解饱和食盐水获取烧碱和氯气:2Cl﹣+2H2O![]() H2↑+Cl2↑+2OH﹣
H2↑+Cl2↑+2OH﹣
C. 向氢氧化钡溶液中加入稀硫酸:Ba2++OH﹣+H++SO42﹣═BaSO4↓+H2O
D. 碳酸钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有H+、Mg2+、NH4+、Al3+、Fe3+、CO32—、SO42—、NO3—中的几种。若加入锌粒,产生无色无味的气体;若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示。则下列说法不正确的是

A. 溶液中的阳离子有H+、Mg2+、NH4+、Al3+
B. 溶液中n(Al3+)=0.1 mol
C. 溶液中一定不含CO32—,可能含有SO42—和NO3—
D. n(H+)∶n(Al3+)∶n(Mg2+)=2∶2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等。在光照条件下,氯气和氢气反应过程如下:
![]()
(1)写出氯元素的原子结构示意图________反应②中形成的化合物的电子式为_________;反应③中被破 坏的化学键属于________键。
(2)在短周期主族元素中,氯元素及与其相邻元素的原子半径从大到小的顺序是________________。
(3)与氯元素同周期且金属性最强的元素在周期表中的位置为________________。
(4)卤素单质及化合物在许多性质上都存在着递变规律。下列有关说法正确的是________________。
a.卤化银的颜色按 AgCl、AgBr、AgI 的顺序依次加深
b.卤化氢的键长按 H—F、H—C1、H—Br、H—I 的顺序依次减小
c.卤化氢的还原性按 HF、HCl、HBr、HI 的顺序依次增强
d.卤素单质与氢气化合按 F2、C12、Br2、I2 的顺序由难变易
(5)卤素单质的键能大小如图。由图推断:

①非金属性强的卤素,其单质分子的化学键_____ 断裂(填“容易”或“不容易”或“不一定容易”)。
②卤素单质键能大小与键长的关系为:________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com