
【题目】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌.某含锌矿的主要成分为ZnS(还含少量FeS等其他成分),以其为原料冶炼锌的工艺流程如图所示: 
回答下列问题:
(1)硫化锌精矿的焙烧在氧气气氛的沸腾炉中进行,所产生焙砂的主要成分的化学式为 .
(2)焙烧过程中产生的含尘烟气可净化制酸,该酸可用于后续的操作.
(3)浸出液“净化”过程中加入的主要物质为 , 其作用是 .
(4)电解沉积过程中的阴极采用铝板,阳极采用Pb﹣Ag合金惰性电极,阳极逸出的气体是 .
(5)改进的锌冶炼工艺,采用了“氧压酸浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质.“氧压酸浸”中发生的主要反应的离子方程式为 .
【答案】
(1)ZnO
(2)浸出
(3)Zn粉;置换出Fe等
(4)O2
(5)2ZnS+4H++O2=2Zn2++2S↓+2H2O
【解析】解:硫化锌精矿的焙烧可生成ZnO、氧化铁等,含尘烟气含有含硫氧化物,可用于制备硫酸,浸出液加入硫酸可生成硫酸锌、硫酸铁,加入过量锌充分反应,可置换出铁,滤液中主要含有硫酸锌,经电解可得到锌和硫酸,电解液中含有硫酸,可循环利用,(1)含锌矿的主要成分是ZnS,与空气中氧气发生氧化还原反应,则焙砂的主要成分为ZnO,所以答案是:ZnO;(2)焙烧生成的含硫氧化物可转换为硫酸,用于后续的浸出操作,所以答案是:浸出;(3)该含锌矿中还含有FeS等杂质,浸出操作后转化为亚铁离子,可加入锌粉出去亚铁离子,从而出去Fe,所以答案是:Zn粉;置换出Fe等;(4)电解沉积过程中,是电解ZnSO4 , 阳极发生氧化反应,产物为O2 , 所以答案是:O2;(5)“氧压酸浸”法顾名思义,可知反应物中含有H+和O2 , 可以获得非金属单质S,化学方程式为2ZnS+4H++O2=2Zn2++2S↓+2H2O,所以答案是:2ZnS+4H++O2=2Zn2++2S↓+2H2O.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图表示小麦开花数天后测定种子中主要物质的变化,请据图回答下列问题:

(1)成熟小麦种子中主要的营养物质是________。
(2)检测还原糖的试剂是________,还原糖的多少可通过________来判断。
(3)小麦种子成熟过程中,胚乳里蔗糖与还原糖含量比较,两者的变化趋势________________(填“相同”或“不同”)。
(4)种子成熟时,淀粉的形成与一种磷酸化酶的活性有密切关系,为验证磷酸化酶是否是蛋白质,实验过程中实验组试管加入________,对照组试管中加入2 mL豆浆,然后加入等量的________,如果均出现________现象,则证明磷酸化酶是蛋白质。
(5)播种等量的小麦种子和花生种子,________种子需要浅播,因为该种子中_______化合物含量多,该化合物元素组成特点是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列化学用语或化学原理的理解和描述均正确的是( )
A.电子式 ![]() 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子
B.比例模型 ![]() 可以表示二氧化碳分子,也可以表示水分子
可以表示二氧化碳分子,也可以表示水分子
C.明矾能水解生成Al(OH)3胶体,可用作饮用水杀菌
D.原子结构示意图 ![]() 可以表示12C,也可以表示14C
可以表示12C,也可以表示14C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳纤维强化塑料是一种新型的高强度复合材料,其强度比钢铁材料大而密度比铝小。据报道,每架波音767飞机使用了1吨碳纤维材料,而一种新型的波音757飞机使用了9吨以上的碳纤维。制取碳纤维的一种方法是将聚丙烯腈纤维在稀有气体中进行高温处理而获得,这种碳纤维的结构可表示如下:
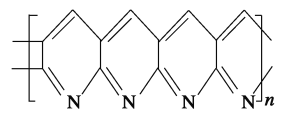
(1)构成这种碳纤维的元素是______,其原子个数比为_________。
(2)用乙炔和HCN为原料合成这种碳纤维的流程可表示如下:
CH≡CH![]() A
A![]() B
B![]() C
C![]() 碳纤维
碳纤维
用化学方程式表示以下过程:
①CH≡CH和HCN反应_______________________;
②A―→B________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酰胺66常用于生产帐篷、渔网、降落伞及弹力丝袜等织物,可利用下列路线合成:
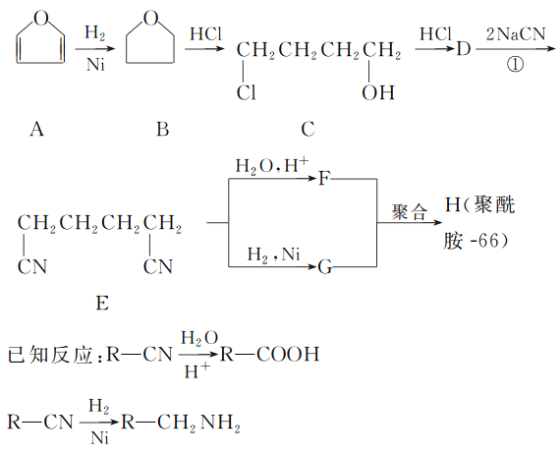
(1)能与银氨溶液反应的B的同分异构体的结构简式为________。
(2)D的结构简式为________;①的反应类型为________。
(3)为检验D中的官能团,所用试剂包括NaOH水溶液及________。
(4)由F和G生成H的反应方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是( )
A. CuCl2 B. MgCl2 C. FeCl2 D. FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+ (aq)+SCN﹣(aq) ![]() Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( )
Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( ) 
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN﹣(aq)=Fe(SCN)2+(aq)△H>0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2 , 则K1>K2
C.反应处于D点时,一定有V正>V逆
D.A点与B点相比,A点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁镍蓄电池,放电时的总反应为:Fe+Ni2O3+3H2O ![]() Fe(OH)2+2Ni(OH) 2下列有关该电池的说法不正确的是( )
Fe(OH)2+2Ni(OH) 2下列有关该电池的说法不正确的是( )
A.电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe
B.电池放电时,负极反应为Fe+2OH﹣﹣2e﹣═Fe(OH)2
C.电池充电过程中,阴极附近溶液的pH降低
D.电池充电时,阳极反应为2Ni(OH)2+2OH﹣﹣2e﹣═Ni2O3+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将含有0.1molSiO2的铝、硅混合物分别与足量NaOH溶液、盐酸混合,充分反应后前者可得到11.2L气体(标准状况),后者可得到6.72L气体(标准状况),则参加反应的n(HCl)与n(NaOH)之比为( )
A.1:1
B.1:2
C.2:1
D.3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com