
����Ŀ��̼��άǿ��������һ�����͵ĸ�ǿ�ȸ��ϲ��ϣ���ǿ�ȱȸ������ϴ���ܶȱ���С���ݱ�����ÿ�ܲ���767�ɻ�ʹ����1��̼��ά���ϣ���һ�����͵IJ���757�ɻ�ʹ����9�����ϵ�̼��ά����ȡ̼��ά��һ�ַ����ǽ��۱�ϩ����ά��ϡ�������н��и��´�������ã�����̼��ά�Ľṹ�ɱ�ʾ���£�
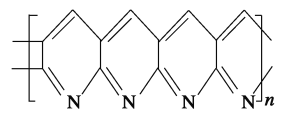
(1)��������̼��ά��Ԫ����______����ԭ�Ӹ�����Ϊ_________��
(2)����Ȳ��HCNΪԭ�Ϻϳ�����̼��ά�����̿ɱ�ʾ���£�
CH��CH![]() A
A![]() B
B![]() C
C![]() ̼��ά
̼��ά
�û�ѧ����ʽ��ʾ���¹��̣�
��CH��CH��HCN��Ӧ_______________________��
��A�D��B________________________________��
���𰸡�(1)C��H��N 3��1��1
(2)��CH��CH��HCN![]() CH2===CH��CN
CH2===CH��CN
��nCH2===CH��CN![]()

��������̼��ά������һ����Ҫ�������ϲ��ϣ���Ŀ��֪������ȡ����̼��ά�ǽ��۱�ϩ�澭���´������ã��۱�ϩ��ĽṹΪ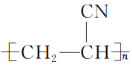 ��ע����̼��ά�Ľṹ�����Խ��۱�ϩ��ṹдΪ
��ע����̼��ά�Ľṹ�����Խ��۱�ϩ��ṹдΪ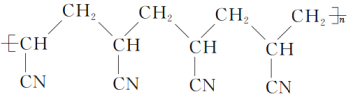 ���С�CN�ĽṹΪ��C��N�����ֱ任д���ǽ����Ĺؼ�һ������������������ʾ���۱�ϩ�澭������Ӧ���̼��ά����һ�����´�����Ӧ���������ṹ�Ļ����Ͻ������C��N�е����������½�Ϲ��ɻ�״�ṹ��������C��C�ڴ������������⣬��C�л�״�ṹ�ġ�CH2����
���С�CN�ĽṹΪ��C��N�����ֱ任д���ǽ����Ĺؼ�һ������������������ʾ���۱�ϩ�澭������Ӧ���̼��ά����һ�����´�����Ӧ���������ṹ�Ļ����Ͻ������C��N�е����������½�Ϲ��ɻ�״�ṹ��������C��C�ڴ������������⣬��C�л�״�ṹ�ġ�CH2����![]() �ϸ���ȥһ����ԭ�Ӷ��γ�CC˫���ṹ���γ�̼��ά����Ȼ���ڡ�CH2��ԭ��������ȥһ����ԭ�Ӻ���һ����ԭ�ӣ����Կ�֪����̼��ά��C��H��N����Ԫ�ع��ɣ��������е�һ�������ṹ��Ԫ
�ϸ���ȥһ����ԭ�Ӷ��γ�CC˫���ṹ���γ�̼��ά����Ȼ���ڡ�CH2��ԭ��������ȥһ����ԭ�Ӻ���һ����ԭ�ӣ����Կ�֪����̼��ά��C��H��N����Ԫ�ع��ɣ��������е�һ�������ṹ��Ԫ ���ɿ���C��H��N����ԭ�ӵĸ�����ӦΪ3��1��1��
���ɿ���C��H��N����ԭ�ӵĸ�����ӦΪ3��1��1��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������״̬�£��ܵ���ĵ������( )
A.��ˮ
B.�����ƹ���
C.������̼ˮ��Һ
D.���ڵ��Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ե���ʵ�������ȷ����(����)
A. ����ˮ��õ�����Һ�ܵ��������
B. �Ȼ�������ˮ�ܵ��磬��Һ̬�Ȼ��ⲻ�ܵ���
C. NaCl�ǵ���ʹ�NaCl�����ܵ���
D. NaCl��Һ�ڵ��������µ����Na����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ӵ��γɹ���ʾ��ͼ(����ͼ)�ش����⣺

(1)H��H���ļ���Ϊ________���١����У���ϵ�����ɸߵ��͵�˳����________��
(2)����˵������ȷ����( )
A�����������к���һ���м�
B���ɢٵ��ܣ������ں˼���ֵļ�������
C���ɢܵ��ݣ�����������������
D�����������к���һ�����Թ��ۼ�
(3)���ֳ�����ѧ���ļ������±���
��ѧ�� | Si��O | H��O | O==O | Si��Si | Si��C |
����/kJ��mol��1 | 460 | 464 | 498 | 176 | x |
��ش��������⣺
�ٱȽ�Si��Si����Si��C���ļ��ܴ�С��x________(�>������<������)176��
��H2����Ϊ21���������������ȼ�ϣ������п�ѧ��������ǡ�21���͵���Դ������δ����ʯ�͡��Ĺ۵㡣�Լ��㣺ÿǧ��H2ȼ��(����ˮ����)�ų�������ԼΪ________��ÿĦ������ȫȼ�շų�������ԼΪ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ԫ�ػ�̬ԭ�ӵĵ����Ų������ж�Ԫ��,���ش����⡣
AԪ�ص�ԭ����ֻ��һ���ܲ���ֻ��1������;BԪ�ص�ԭ��3p����ϵõ�1�����Ӻ�����������������;CԪ�ص�ԭ�ӵ�2p�������1�����ӵ������������������ӵ����������෴;DԪ�ص�ԭ�ӵ����ܲ�����8������,�����ܲ���ֻ��1������;EԪ��ԭ�ӵ���Χ�����Ų�Ϊ3s23p6��
(1)д����A��B��C��D�е�����Ԫ����ɵĻ�����Ļ�ѧʽ: (����д��5��)��
(2)д��������Ԫ����ɵ������Ƶ�A�ĵ��ʵĻ�ѧ����ʽ: ��
(3)����ij��Һ���Ƿ���D+,��ͨ�� ��Ӧ��ʵ��;����ij��Һ���Ƿ���B-,ͨ�����õ��Լ��� �� ��
(4)д��E��Ԫ�ط���: ,Ҫ֤��̫�����Ƿ���EԪ��,�ɲ��õķ����� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ЧӦ����ȫ���ע�Ļ�������֮һ��CO2��Ŀǰ�����к�����ߵ�һ���������壮��ˣ����ƺ�����CO2�ǽ������ЧӦ����Ч;����
��1�����д�ʩ�У������ڽ��ʹ�����CO2Ũ�ȵ��У� �� ������ĸ�� a�����ٻ�ʯȼ�ϵ�ʹ��
b��ֲ�����֣�����ֲ�����
c�����ý��ܼ���
d������̫���ܡ�����
��2����CO2ת�����л������Чʵ��̼ѭ����CO2ת�����л�������Ӻܶ࣬�磺 a��6CO2+6H2O ![]() C6H12O6+6O2
C6H12O6+6O2
b��CO2+3H2 ![]() CH3OH+H2O
CH3OH+H2O
c��CO2+CH4 ![]() CH3COOH
CH3COOH
d��2CO2+6H2 ![]() CH2�TCH2+4H2O
CH2�TCH2+4H2O
���Ϸ�Ӧ�У�����ܵ��� �� ԭ����������ߵ��� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��п��һ��Ӧ�ù㷺�Ľ�����Ŀǰ��ҵ����Ҫ���á�ʪ��������ұ��п��ij��п�����Ҫ�ɷ�ΪZnS����������FeS�������ɷ֣�������Ϊԭ��ұ��п�Ĺ���������ͼ��ʾ�� 
�ش��������⣺
��1����п����ı������������յķ���¯�н��У���������ɰ����Ҫ�ɷֵĻ�ѧʽΪ ��
��2�����չ����в����ĺ��������ɾ������ᣬ��������ں�����������
��3������Һ�������������м������Ҫ����Ϊ �� �������� ��
��4�������������е������������壬��������Pb��Ag�Ͻ���Ե缫�������ݳ��������� ��
��5���Ľ���пұ�����գ������ˡ���ѹ�������ȫʪ�����̣���ʡ�������¿�����Ⱦ�ı��չ��̣��ֿɻ��һ���й�ҵ��ֵ�ķǽ������ʣ�����ѹ������з�������Ҫ��Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ҵ����۷е�Ⱥ���̼ͬԭ�ӵ��������۷е�ߵ���Ҫԭ���ǣ� ��
A.�Ҵ��ķ������Ⱥ���̼ͬԭ�ӵ������ķ�������
B.�Ҵ�����֮�����γ����
C.̼ԭ������ԭ�ӵĽ��û��̼ԭ������ԭ�ӵĽ�ϵij̶ȴ�
D.�Ҵ���Һ�壬������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Rm+��Xn-������ͬ�ĵ��Ӳ�ṹ�����������뾶��С��ϵΪ�� ��
A. ǰ�ߴ��ں���B. ǰ��С�ں���C. ǰ�ߵ��ں���D. ����ȷ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com