
【题目】按照下列元素基态原子的电子排布特征判断元素,并回答问题。
A元素的原子中只有一个能层且只含1个电子;B元素的原子3p轨道上得到1个电子后不能再容纳外来电子;C元素的原子的2p轨道上有1个电子的自旋方向与其他电子的自旋方向相反;D元素的原子第三能层上有8个电子,第四能层上只有1个电子;E元素原子的外围电子排布为3s23p6。
(1)写出由A、B、C、D中的三种元素组成的化合物的化学式: (至少写出5个)。
(2)写出用上述元素组成的物质制得A的单质的化学方程式: 、
(3)检验某溶液中是否含有D+,可通过 反应来实现;检验某溶液中是否含有B-,通常所用的试剂是 和 。
(4)写出E的元素符号: ,要证明太阳上是否含有E元素,可采用的方法是 。
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇及稀硫酸,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂.实验室拟以下列方法制取CuCl:在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl.试回答以下问题:
(1)CuCl制备过程中需配制物质的量浓度为2.0mol/L的CuSO4溶液. ①配制950mL 2.0mol/L的CuSO4溶液应称取胆矾的质量为g.
②某学生实际配制CuSO4溶液的浓度为1.8mol/L,原因可能是 .
A.托盘天平的砝码生锈 B.容量瓶中原来存有少量蒸馏水
C.溶解后的烧杯未经多次洗涤 D.胶头滴管加水定容时仰视刻度
(2)写出用上述方法制备CuCl的离子方程式 .
(3)在上述制取过程中,经过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品.其中“于70℃真空干燥”的目的是; . (回答两点)
(4)据世界卫生组织统计,最常用的避孕环含金属铜,避孕过程中生成了CuCl.其原因是铜与人体分泌物中的盐酸以及子宫内的空气反应:Cu+HCl+O2=CuCl+HO2 , HO2(超氧酸) 不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是 .
A.氧化产物是HO2
B.HO2在碱中能稳定存在
C.HO2 的电离方程式是HO2H++O2﹣
D.1mol Cu 参加反应有2mol电子发生转移.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组利用荧光素—荧光素酶生物发光法,测定人参愈伤组织中ATP的含量,以研究人参细胞能量代谢的特点。
实验原理:荧光素在荧光素酶、ATP等物质参与下,进行反应发出荧光;用分光光度计可测定发光强度;当荧光素和荧光素酶都足量时,在一定范围内,ATP的含量与发光强度成正相关。
实验步骤:
一、ATP的提取:称取一定量的人参愈伤组织,研磨后沸水浴10min,冷却至室温,离心,取上清液。
二、ATP的测定:吸取一定量的上清液,放入分光光度计反应室内,并注入适量的所需物质,在有氧等适宜条件下进行反应,记录发光强度并计算ATP含量。
请回答:
(1)步骤一中的沸水浴处理,使酶的 被破坏而失活。
(2)步骤二注入的物质中,属于反应物的是 。分光光度计反应室内能量的转换形式是 。
(3)荧光素酶价格昂贵,为能准确测定出ATP的含量,又能节省酶的用量,学习小组探究了“测定ATP时所需荧光素酶溶液的最佳浓度”,实验结果如图。

①学习小组配制了1×10-8mol/LATP标准液、 和70mg/L的荧光素溶液(过量)进行实验。
②结果表明:
图中 点所对应的荧光素酶浓度为最佳浓度。
图中e、f、g点所对应的荧光素酶浓度不同,但发光强度相同,这是因为 。
(4)ATP测定对食品卫生监控有重要意义。食品卫生检验人员利用上述生物发光法测定某熟食品样品中细菌的ATP总含量,测算出了细菌的数量,从而判断食品污染程度。做出上述判断的理由是:每个细菌细胞中ATP的含量 。
(5)下列生理过程中,不消耗ATP的一组是( )
A.蛋白质的合成和加工 B.染色体的复制和运动
C.胰岛素的分泌 D.植物细胞的质壁分离和复原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列化学用语或化学原理的理解和描述均正确的是( )
A.电子式 ![]() 可以表示羟基,也可以表示氢氧根离子
可以表示羟基,也可以表示氢氧根离子
B.比例模型 ![]() 可以表示二氧化碳分子,也可以表示水分子
可以表示二氧化碳分子,也可以表示水分子
C.明矾能水解生成Al(OH)3胶体,可用作饮用水杀菌
D.原子结构示意图 ![]() 可以表示12C,也可以表示14C
可以表示12C,也可以表示14C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列科研成果不是由我国发明或创造的是( )
A. 发现元素周期律
B. 抗疟药青蒿素和双氢青蒿素的发现
C. 世界上首次人工合成的酵母丙氨酸转移核糖核酸
D. 世界上第一个由人工合成的具有生理活性的蛋白质——结晶牛胰岛素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳纤维强化塑料是一种新型的高强度复合材料,其强度比钢铁材料大而密度比铝小。据报道,每架波音767飞机使用了1吨碳纤维材料,而一种新型的波音757飞机使用了9吨以上的碳纤维。制取碳纤维的一种方法是将聚丙烯腈纤维在稀有气体中进行高温处理而获得,这种碳纤维的结构可表示如下:
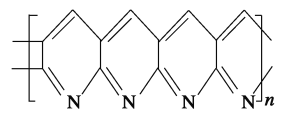
(1)构成这种碳纤维的元素是______,其原子个数比为_________。
(2)用乙炔和HCN为原料合成这种碳纤维的流程可表示如下:
CH≡CH![]() A
A![]() B
B![]() C
C![]() 碳纤维
碳纤维
用化学方程式表示以下过程:
①CH≡CH和HCN反应_______________________;
②A―→B________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚酰胺66常用于生产帐篷、渔网、降落伞及弹力丝袜等织物,可利用下列路线合成:
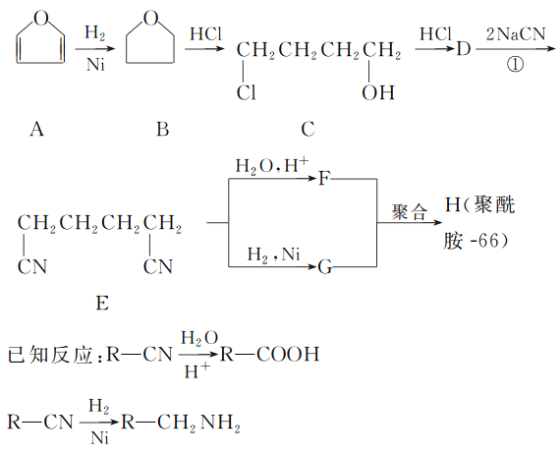
(1)能与银氨溶液反应的B的同分异构体的结构简式为________。
(2)D的结构简式为________;①的反应类型为________。
(3)为检验D中的官能团,所用试剂包括NaOH水溶液及________。
(4)由F和G生成H的反应方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)FeCl3(aq)与KSCN(aq)混合时存在下列平衡:Fe3+ (aq)+SCN﹣(aq) ![]() Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( )
Fe(SCN)2+ (aq);已知平衡时,物质的量浓度c[Fe(SCN)2+]与温度T的关系如下图所示,则下列说法正确的是( ) 
A.FeCl3(aq)与KSCN(aq)反应的热化学反应方程式为:Fe3+(aq)+SCN﹣(aq)=Fe(SCN)2+(aq)△H>0
B.温度为T1、T2时,反应的平衡常数分别为K1、K2 , 则K1>K2
C.反应处于D点时,一定有V正>V逆
D.A点与B点相比,A点的c(Fe3+)大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生血液化验单中“萄萄糖”的结果为5.04×10-3mol/L。这里“5.04×10-3mol/L”表示葡萄糖的( )
A. 物质的量 B. 摩尔质量 C. 质量分数 D. 物质的量浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com