
【题目】在 2 L的密闭容器中, 充入 1 mol N2 和 3 mol H2, 在一定的条件下反应, 2 分钟后达到平衡状态, 相同温度下, 测得平衡时混合气体的压强比反应前混合气体的压强减小了 1/10, 求:
(1) 平衡时混合气体中三种气体的物质的量比为多少______?
(2) N2 的转化率为多少 _____?
(3) 该温度下的平衡常数为多少_____ ?
【答案】2:6:1 20% 0.06(或5.8×10-2)(L/mol )2
【解析】
令参加反应的氮气的物质的量为nmol,根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量。
(1)根据压强之比等于物质的量之比,列方程求出n的值,进而计算平衡时混合气体中三种气体的物质的量比;
(2)根据转化率的定义计算;
(3)根据K=![]() 计算。
计算。
根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量。
令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ![]() 2NH3 ,
2NH3 ,
开始(mol): 1 3 0
变化(mol): n 3n 2n
平衡(mol): 1-n 3-3n 2n
压强之比等于物质的量之比,所以(1-n+3-3n+2n)mol=(1+3)mol×(1-![]() ),解得n=0.2,
),解得n=0.2,
(1)平衡时n(N2)=(1-n)mol=(1-0.2)mol=0.8mol;平衡时n(H2)=(3-3n)mol=(3-3×0.2)mol=2.4mol;平衡时n(NH3)=2n=0.2mol×2=0.4mol;所以,平衡时混合气体中N2、H2、NH3三种气体的物质的量比为0.8mol:2.4mol:0.4mol=2:6:1;
(2)N2 的转化率为![]() ×100%=20%;
×100%=20%;
(3)该温度下达平衡时混合气体中N2、H2、NH3三种气体的物质的量浓度分别为0.4mol/L、1.2mol/L、0.2mol/L,平衡常数K=![]() =
=![]() (L/mol )2。
(L/mol )2。


科目:高中化学 来源: 题型:
【题目】下列化学方程式书写错误的是( )
A. Na2CO3+2HCl= 2NaCl+H2O+CO2↑B. CO2+Ca(OH)2=CaCO3↓+H2O
C. CuSO4+ BaOH=CuOH↓+BaSO4D. 3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。实验步骤如下:

①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液褪色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
(1)A试管中发生反应的化学方程式为__________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_____。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将实验后的溶液分成两份,分别滴加氯水和氨水,均产生白色沉淀。写出其中SO2表现还原性的离子反应方程式为_____。
(4)下列对导管E作用的分析中正确的是__________。
A 加热过程中,可上下移动导管E,起搅拌作用
B 停止加热,试管内的压强减少,从导管E进入的空气可增大试管A内的压强,防止倒吸
C 停止反应,撤装置之前往导管E中通入空气,可排出装置内的SO2气体,防止其污染环境
II ClO2与Cl2的氧化性相近,可用于自来水消毒和果蔬保鲜等方面。某兴趣小组通过图1装置(夹持装置略)对ClO2的制备、除杂、吸收和释放等进行了研究。

(1)仪器B的名称是________。打开B的活塞,A中发生反应为:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O,为使ClO2在D中被稳定剂充分吸收,滴加B中稀盐酸的速度宜______(填“快”或“慢”)。
(2)关闭B的活塞,ClO2在D中被某种稳定剂完全吸收生成NaClO2,此时F中溶液颜色不变,则装置C的作用是____。
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_____;在ClO2释放实验中,打开E的活塞,D中发生反应,则此时装置F的作用是_____。安装F中导管时,应选用图2中的____(填“a”或“b”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)![]() cC(g)表示]化学平衡的影响,得到如图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):
cC(g)表示]化学平衡的影响,得到如图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率):

分析图象,回答下列问题:
(1)在图象反应Ⅰ中,此正反应为________(填“吸热”或“放热”)反应,若p1>p2,则此反应的△S________0(填“>”或“<”),由此判断,此逆反应自发进行,必须满足的条件是____________.
(2)在图象反应Ⅱ中,T1_____T2(填“>”“<”或“=”),该正反应为_______(填“吸热”或“放热”)反应.
(3)在图象反应Ⅲ中,若T1<T2,则该反应_______(填“能”或“不能”)自发进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示,其中W原子的最外层电子数是最内层电子数的3倍。下列判断正确的是
![]()
A. 原子半径:r(W)>r(Z)>r(Y)>r(X)
B. Y元素的单质只能跟酸反应,不能跟碱反应
C. 最简单气态氢化物的热稳定性:W>Z
D. W元素的各种氧化物对应的水化物均为强酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由合成气制备二甲醚,涉及如下反应:
(i)2CH3OH(g)![]() C2H4(g)+2H2O(g) ΔH1
C2H4(g)+2H2O(g) ΔH1
(ii)2CH3OH(g)![]() CH3OCH3(g)+H2O(g) ΔH2
CH3OCH3(g)+H2O(g) ΔH2
能量变化如图所示:
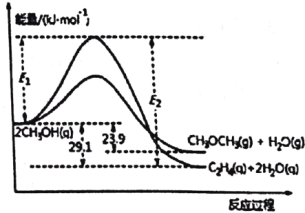
下列说法正确的是
A. ΔH1<ΔH2
B. 反应(ii)为吸热反应
C. C2H4(g)+H2O(g)![]() CH3OCH3(g) ΔH = -5.2 kJ·mol-1
CH3OCH3(g) ΔH = -5.2 kJ·mol-1
D. 若在容器中加入催化剂,则E2-E1将变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如右,电解总反应为:2Cu+H2O![]() Cu2O+H2↑。下列说法正确的是
Cu2O+H2↑。下列说法正确的是

A. 石墨电极上产生氢气
B. 铜电极发生还原反应
C. 铜电极接直流电源的负极
D. 当有0.1 mol电子转移时,有0.1 mol Cu2O生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com