
【题目】如图为元素周期表的一部分,已知D为金属元素且其原子核外内层电子数为最外层电子数的5倍
A | B | C | ||||
D | E | X | ||||
G | ||||||
Y |
请回答下列问题:
(1)元素B在元素周期表中的位置为________
(2)元素A和元素E的最简单氢化物中沸点较高的是_____(填化学式)
(3)已知BC2中所有原子的最外层均满足8电子稳定结构,则BC2的电子式为_____其中B元素的化合价为______价。
(4)D3A2与H2O反应可生成两种碱,请写出该反应的化学方程式____________
(5)Y与X的原子序数之差为____________.
【答案】第二周期第VIA族 NH3 ![]() +2 Mg3N2+8H2O=3Mg(OH)2↓+2NH3·H2O 36
+2 Mg3N2+8H2O=3Mg(OH)2↓+2NH3·H2O 36
【解析】
D为金属元素且其原子核外内层电子数为最外层电子数的5倍,则D为Mg,根据元素在周期表中的位置可知:A为N;B为O;C为F;E为P;X为Ar;G为Kr;Y为Xe,据此分析解答。
(1)元素B为O,处于第二周期VIA族,故答案为:第二周期第VIA族;
(2)元素A和元素E的最简单氢化物分别为PH3和NH3,因氨气分子间存在氢键导致其沸点较高,故答案为:NH3;
(3) BC2为OF2,电子式为:![]() ,因F的非金属性比O强,在该化合物中F为-1价,O为+2价,故答案为:
,因F的非金属性比O强,在该化合物中F为-1价,O为+2价,故答案为:![]() ;+2;
;+2;
(4)D3A2为Mg3N2与H2O反应可生成两种碱分别为氢氧化镁和一水合氨,反应为:Mg3N2+8H2O=3Mg(OH)2↓+2NH3·H2O,故答案为:Mg3N2+8H2O=3Mg(OH)2↓+2NH3·H2O;
(5) X为Ar,原子序数为18;Y为Xe,原子序数为54,两者原子序数差为36,故答案为:36;


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
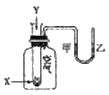
【题目】某学生用如图所示装置进行化学反应X+Y=Z能量变化情况的研宄。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述:①该反应为放热反应②生成物的总能量比反应物更高③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来,其中正确的是( )
A.①②③
B.①③
C.①②
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅晶体是立体的网状结构,其结构如图所示。
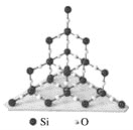
下列关于二氧化硅晶体的说法不正确的是( )
A. 晶体中每个硅原子与4个氧原子相连
B. 晶体中硅、氧原子个数比为1∶2
C. 晶体中最小环上的原子数为8
D. 晶体中共用一个硅原子的最小的环的原子数目为12
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T°C时,将6mol A(g)和2molB(g)充入2L的恒容密闭容器中发生反应:3A(g)+B(g)mC(g)+2D(s)。测得2s内C(g)的平均反应速率为0.3 mol·L-1·s-1,且2s末D(g)的物质的量为1.2 mol。
请回答下列问题:
(1)m=_____
(2)2s内用物质A表示的平均反应速率为______。
(3)2s末时物质B的转化率为_____
(4)从2s末开始到C的浓度变为1.2 mol·L-1时所用的时间____2s(填"大于”“小于”或”等于”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质是含钠元素的单质或化合物,其中B为淡黄色固体,它们有如图所示的转化关系:
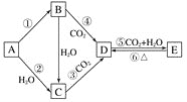
(1)推断各符号所代表的物质的化学式:A__,B__,C__,D__,E__。
(2)写出反应②的化学方程式:___。
(3)向D的饱和溶液中通入CO2时,反应的化学方程式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在甲、乙、丙三个恒温恒容的密闭容器中,分别加入足量活性炭和一定量的 NO,进行反应C(s)+2NO(g) ![]() N2(g)+CO2(g),测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
N2(g)+CO2(g),测得各容器中 c(NO)随反应时间 t 的变化情况如下表所示,下列说法正确的是( )
容器(温度) | 0min | 40min | 80min | 120min | 160min | |
甲(400℃) | c(NO) | 2.00 mol/ L | 1.50 mol/ L | 1.10 mol/ L | 0.80 mol/ L | 0.80 mol/ L |
乙(400℃) | c(NO) | 1.00 mol/ L | 0.80 mol/ L | 0.65 mol/ L | 0.53 mol/ L | 0.45 mol/ L |
丙(T℃) | c(NO) | 2.00 mol/ L | 1.40 mol/ L | 1.10 mol/ L | 1.10 mol/ L | 1.10 mol/ L |
A.达到平衡状态时,2v正(NO)= v逆(N2)
B.活性炭的质量不再改变不能说明反应已达平衡状态
C.丙容器中,从反应开始到建立平衡时的平均反应速率为v(NO) >0.01125 mol·L-1·min-1
D.由表格数据可知:T<400℃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,反应如下:CO(g)+2H2(g)=CH3OH(g)。在2L密闭容器中充入物质的量之比为1:2的CO和H2,在催化剂作用下充分反应.测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如下图所示。下列说法正确的是
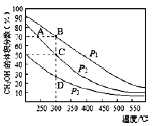
A.该反应的△H<O,且p1<p2<p3
B.在C点时,H2转化率为75%
C.反应速率:v逆(状态A)>v逆(状态B)
D.在恒温恒压条件下,向该密闭容器中再充入1molCH3OH,
达平衡时CH3OH的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《 Journal of Energy Chemistry》报导我国科学家设计CO2熔盐捕获与转化装置如图。下列有关说法正确的是

A. a为负极
B. 熔盐可用KOH溶液代替
C. d极电极反应式为CO32-+4e-===C+3O2-
D. 转移lmol电子可捕获CO211.2L(标况下)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸四氨合铜晶体([Cu(NH3)4]SO4·H2O)常用作杀虫剂、媒染剂。实验室拟用废旧印刷电路板(含有Cu、Fe、Al、Zn)制备该晶体,具体流程如下:

已知:硫酸四氨合铜易溶于水,不溶于乙醇、四氯化碳等有机溶剂;常温下,硫酸四氨合铜在空气中易与水和二氧化碳反应,受热时易失氨。
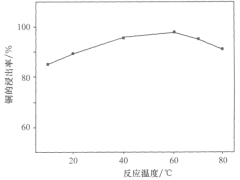
(1)某科研小组选取一定量的稀硝酸和稀硫酸的混合酸溶解废旧印刷电路板时,得出温度与铜的浸出率关系如图所示。步骤①中采用合适的加热方式是___;温度越高,铜的浸出率反而下降,原因可能是___。
(2)步骤②、③需要的玻璃仪器有___;检验“水相Ⅱ”中是否含有Fe3+所需试剂为___。
(3)步骤④中氨水必须适当过量的原因是___。
(4)步骤⑥的具体操作为___。
(5)样品中NH3含量测定:实验装置如图所示,称取0.3400g样品放入圆底烧瓶中,加入80mL水溶解,再加入10%NaOH溶液10.00mL。在锥形瓶中,准确加入0.5000mol·L-lHC1标准溶液36.00mL,放入冰水浴中冷却。先大火后小火加热烧瓶,并保持微沸1h左右。取出插入HC1溶液中的导管,从冰水浴中取出锥形瓶,滴加2滴0.1%甲基红溶液,用0.5000mol·L-1NaOH标准溶液滴定剩余溶液,消耗NaOH标准溶液28.00mL。

样品中NH3的质量分数为___(保留两位有效数字),实验检测结果比理论值偏小的原因可能是___(写一种可能原因)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com