
| A、Na2SO4 |
| B、AgNO3 |
| C、NaCl |
| D、AlCl3 |


科目:高中化学 来源: 题型:
| A、钠块沉在乙醇液面的下面 |
| B、反应较为和缓 |
| C、钠块在乙醇的液面上游动 |
| D、钠块表面有气体放出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A与B互为同分异构体 |
| B、A与B的分子组成相差n个“CH2” |
| C、A与B的分子组成相差n个“CO2” |
| D、A与B的分子组成相差n个“H2O” |
查看答案和解析>>
科目:高中化学 来源: 题型:
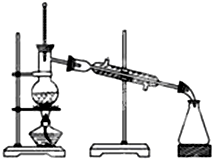 地球是一个巨大的生态系统,森林对保护改善人类的生存环境有着十分重要的作用.科学实验证明,1公顷柳杉林每月可以吸收SO2160kg,试解答下列问题:
地球是一个巨大的生态系统,森林对保护改善人类的生存环境有着十分重要的作用.科学实验证明,1公顷柳杉林每月可以吸收SO2160kg,试解答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
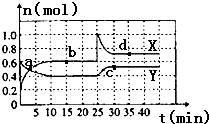 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入容积为2L的恒温密闭容器中,各组分物质的量随时间变化关系如图所示.
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入容积为2L的恒温密闭容器中,各组分物质的量随时间变化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(OH)2 |
| B、NaOH |
| C、H2S |
| D、AgNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
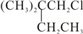 .B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如图所示.
.B和D分别与强碱的醇溶液共热,都只能得到有机化合物E.以上反应及B的进一步反应如图所示.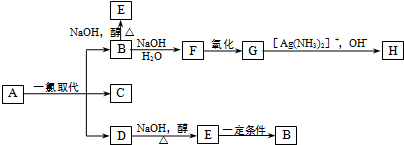
查看答案和解析>>
科目:高中化学 来源: 题型:
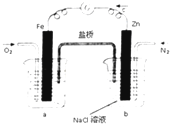
| A、烧杯a中的溶液pH减小 |
| B、烧杯b中发生氧化反应 |
| C、烧杯a中发生的反应为2H++2e-=H2↑ |
| D、烧杯b中发生的反应为2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| CaO(或MgO) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com