
【题目】下列物质中,不含硅酸盐的是
A. 黏土 B. 水玻璃
C. 硅芯片 D. 普通水泥
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
【题目】某原电池构造如图所示,下列说法不正确的是( ) 
A.负极反应为:Cu﹣2e﹣═Cu2+
B.若该原电池工作前两电极质量相等,则工作后,当铜的质量减少6.4g时,两电极质量相差21.6g(假设电解质溶液都是足量的)
C.当铜的质量减小12.8 g时,外电路中通过0.4mol电子
D.原电池的总反应式为:Cu+2AgNO3═2Ag+Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学科学对提高人类生活质量和促进社会发展具有重要作用,下列说法中正确的是( )
A.煤经过气化和液化两个物理变化,可变为清洁能源
B.汽车尾气的大量排放影响了空气的质量,是造成PM2.5值升高的原因之一
C.自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
D.糖类、油脂和蛋白质都能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量氨基甲酸铵(NH2COONH4)加入密闭容器中,发生反应NH2COONH4(s)![]() 2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法不正确的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数(-lgK)值随温度(T)的变化曲线如图所示,下列说法不正确的是
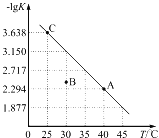
A. 该反应的ΔH>0
B. NH3的体积分数不变时,该反应一定达到平衡状态
C. A点对应状态的平衡常数K(A)=10-2.294
D. 30℃时,B点对应状态的v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A. 将物质的量浓度为10-3mol/L的醋酸和pH=11的NaOH溶液等体积混合后,溶液显碱性
B. 如图表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则HB是强酸
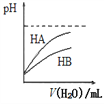
C. 25℃时,pH=2的1.0 L醋酸溶液中水电离出的H+的数目为10-12NA
D. 某吸热反应能自发进行,则该反应一定是熵增的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化能实现的是( )
A.Na ![]() Na2O
Na2O ![]() Na2O2
Na2O2
B.AlCl3 ![]() Al(OH)3
Al(OH)3 ![]() NaAlO2
NaAlO2
C.NaOH ![]() Na2CO3
Na2CO3 ![]() NaHCO3
NaHCO3
D.Fe ![]() FeCl2
FeCl2 ![]() FeCl3
FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学小组学生利用下图所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl36H2O晶体.(图中夹持及尾气处理装置均已略去) 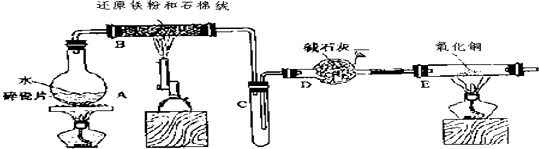
(1)烧瓶底部放置了几片碎瓷片,
碎瓷片的作用是
装置B中发生反应的化学方程式是 .
(2)如果要在C处玻璃管处点燃该气体,则必须对该气体进行 ,
装置E中的现象是 .
(3)停止反应,待B管冷却后,取其中的固体,加入过量盐酸充分反应,过滤.简述检验滤液中Fe3+的操作方法 .
(4)该小组学生利用上述滤液制取FeCl36H2O晶体,设计流程如下:
滤液 ![]() FeCl3溶液
FeCl3溶液 ![]() FeCl36H2O晶体
FeCl36H2O晶体
步骤中通入Cl2的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,0.10mol/LH2A溶液用0.10mol/LNaOH溶液滴定,滴定曲线如下图所示:

已知:①pKa=-lgKa;②二元弱酸H2A的酸式盐NaHA溶液中的c(H+)=![]()
下列说法正确的是
A. 可用甲基橙作滴定指示剂 B. X点溶液pH=6.4
C. 反应H2A+A2-=2HA-的PK=9.7 D. Y点溶液中c(Na+)=c(OH-)+3c(HA-)-c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(GB2760﹣2011)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图1装置(夹持装置略)收集某葡萄酒中SO2 , 并对含量进行测定. 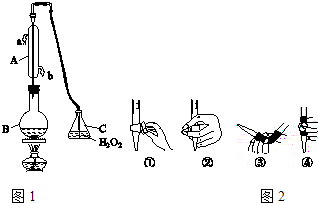
(1)仪器A的名称是 , 水通入A的进口为
(2)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为 .
(3)除去C中过量的H2O2 , 然后用0.0450mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图2中的(填数字编号);若滴定终点时溶液的pH=8.8,则选择的指示剂为
(4)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为:g/L.
(5)该测定结果比实际值偏高的原因是,利用现有装置的改进措施是: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com