
【题目】氧族元素包括氧、硫、硒、碲、钋。
(1)单质硫的同素异形体很多,最常见的是斜方晶硫和单斜晶硫,经过测定,这两种硫的单质都是由S8构成的。S8分子的构型如图所示。S—S键的键角为108°,8个S原子形成两层,每层4个S原子。S8分子中S原子通过 杂化与其他原子成键,斜方晶硫和单斜晶硫中S8分子之间靠 结合在一起。

(2)氧及与其同周期的碳、氮、氟四种原子的第一电离能由大到小的顺序是____________。
(3) 用元素原子电负性的理论判断,H2O中的O—H键的键角 (填“>”、“=”或“<”)H2S中的S—H键的键角。
(4)硒是人体生命活动不可缺少的微量元素,适量的硒能够增强人体免疫力,延缓衰老,清除人体内的有害物质。如图是硒(Se)化锶(Sr)的晶胞模型,据此可知,每个硒化锶晶胞中含有的硒离子为___________个,其化学式为 。

【答案】(1)sp3 分子间作用力(或范德华力) (2)F>N>O>C (3)> (4)4 SrSe
【解析】
试题分析:(1)S8是一个环形分子,每个S与两个其它S原子相连,S原子外层6个电子,两对孤对电子,原子杂化轨道数=δ键数+孤对电子对数=2+(62×1)/2=4,所以S是sp3杂化,斜方晶硫和单斜晶硫中S8分子之间靠分子间作用力结合在一起;
(2)同周期随原子序数增大,元素第一电离能呈增大趋势,N元素原子2p能级容纳3个电子,为半满稳定状态,能量较低,第一电离能高于同周期相邻元素,故第一电离能F>N>O>C;
(3)O的电负性大于S,O与H之间的两对成键电子比S与H之间的两对成键电子更靠近中心原子,因此O与H之间的两对成键电子距离近,排斥力大,键角大;
(4)晶胞中Sr2+离子的个数为12×1/4+1=4,Se2-离子为8×1/8+6×1/2=4,两离子的数目比为1:1,则晶胞的化学式为SrSe。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】铁是人体不可缺少的微量元素,硫玻亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:

(1)实验中用已经准确量取的浓硫酸配制500mL1molL-1的硫酸溶液,则配制时用到的仪器除烧杯、500mL容量瓶外,还需要______、________。
(2)步骤②加入过量氯水后发生反应的离子方程式为______.
(3)步骤④中一系列操作步骤为过滤、洗涤、______、冷却、称量。
(4)某同学发现部分补血剂药片表面发黄,取样品研细,溶于1molL-1的硫酸溶液,过滤.取滤液加______溶液,溶液变红说明该补血剂已部分变质.向变色后的溶液中加入橙汁,溶液红色褪去,说明橙汁含具有______性(填“氧化”或“还原”)的物质.
(5)下列检验(4)中滤液中是否有Fe2+应选用的试剂是______.
A.KSCN溶液B.酸性KMnO4溶液 C.铁粉D.FeCl3溶液.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y![]() 2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
2Z,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3∶2,则Y的转化率最接近于( )
A. 33% B. 40% C. 50% D. 65%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是
A. 分子组成相差一个或几个-CH2—原子团的物质互为同系物,它们的化学性质肯定相似
B. 正丁烷中4个碳原子共直线
C. 甲烷是烷烃中碳含量最低的,也是组成最简单的烃
D. 分子式为C4H10的烃有3种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 甲烷与氯气发生取代反应,只能生成一氯甲烷
B. 乙醇和乙酸都可以与钠反应生成氢气
C. 苯和乙烯均能与溴水发生加成反应使溴水褪色
D. 甲醛易溶于水,其水溶液具有杀菌消毒作用,可用于浸泡海鲜食品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示,电池总反应为:2Ag+Cl2===2AgCl。下列说法正确的是( )

A.正极反应为AgCl+e-===Ag+Cl-
B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙连个探究性学习小组,他们拟测定过氧化钠样品(含少量的Na2O)的纯度。
(1)甲组同学拟选用图l实验装置完成实验:

①写出实验中所发生主要反应的化学方程式____________
②该组同学必须选用的装置的连接顺序是:
A 接(____),(____)接(____), (____)接(____) (填接口字母,可不填满);
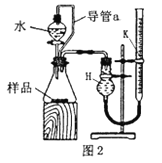
(2)乙组同学仔细分析甲组同学的实验装置后,认为:水滴入锥形瓶中,即使不生成氧气,也会将瓶内空气排出,使所测氧气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氧气体积偏小。于是他们设计了图2所示的实验装置。
①装置中导管a的作用:__________
②实验结束冷却至室温后,在读取量气管k中液面读数时,K中液面高于H中的液面,则测量结果将__________(偏高,不变或偏低),若有影响,应进行_________(操作)后再读效;
③若实验中样品的质量为mg,实验前后量气管k中液面读数分别为V0L、V1L(V0> V1换算成标况)。则样品的纯度为__________(含m、V0、V1的表达式)
(3)图2的装置可测定一定质量铜铁合金(不含其它元素)样品中铁的质量分数。分液漏斗中加入的试剂是__________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com