
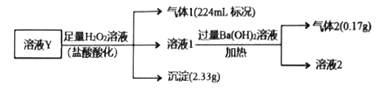
【题目】已知酸性:H2SO3>H2CO3>HSO3->HCO3-。某无色溶液Y可能含有Na+、Fe3+、Ba2+、NH4+、Cl-、SO42-、HCO3-、HSO3-中的几种离子,溶液中阳离子浓度相同。为了确定其组成,某同学进行了如下实验(假设气体均全部逸出,忽略H2O2的分解)。
下列说法不正确的是
A. 溶液Y中一定不存在Fe3+、SO42-
B. 溶液Y中肯定存在HCO3-、HSO3-、Ba2+、NH4+
C. 溶液Y中一定含有Cl-,且n(Cl-)=0.01mol
D. 溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色反应实验验证
【答案】C
【解析】无色溶液Y中一定不存在Fe3+。Y和足量盐酸酸化的双氧水反应生成气体1、溶液1和沉淀,沉淀一定是硫酸钡,则含有Ba2+,因此一定不存在SO42-,一定存在HSO3-,HSO3-被双氧水氧化生成硫酸根,进而生成硫酸钡沉淀,物质的量是0.01mol。气体只能是CO2,所以一定存在HCO3-,物质的量的是0.01mol。溶液1中加入氢氧化钡生成气体和溶液2,则气体一定是氨气,因此一定含有NH4+,物质的量是0.01mol。根据电荷守恒可知溶液中还一定存在Cl-,可能含有Na+。A. 溶液Y中一定不存在Fe3+、SO42-,A正确;B. 溶液Y中肯定存在HCO3-、HSO3-、Ba2+、NH4+,B正确;C. 溶液Y中一定含有Cl-,但由于不能确定是否含有钠离子,则不能计算氯离子的物质的量,C错误;D. 溶液Y中可能存在Na+,为确定其是否存在,可取溶液1通过焰色反应实验验证,D正确,答案选C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】“绿色化学”是当今社会提出的一个新概念。在“绿色化学”工艺中,理想状态是反应中原子全部转化为目标产物,即原子利用率为100%。利用以下各种化学反应类型的合成过程最符合绿色化学的是
A.取代反应 B.水解反应 C.加聚反应 D.缩聚反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下列各组物质按单质、酸、碱、盐分类顺序排列,其中正确的是
A.氯水、盐酸、火碱、硫酸钡
B.水银、硫酸、烧碱、硫酸氢钠
C.铜、醋酸、石灰石、氯化铜
D.臭氧、硝酸、纯碱、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烃A是一种重要的化工原料,A完全燃烧后生成m(CO2):m(H2O)=22:9,A在同系物中相对分子质量最小。现有如下图转化关系:

请回答:
(1)有机物A中含有的官能团名称为_________。
(2)有机物F与氢氧化钠溶液反应的化学方程式为_____________。
(3)有机物E能使溴的四氯化碳溶液褪色,其原因是_________(用化学方程式表示)。
(4)下列说法不正确的是_________
A.B![]() C可通过如下两步直接实现:①热铜丝催化氧化,②直接与新制Cu(OH)2共热
C可通过如下两步直接实现:①热铜丝催化氧化,②直接与新制Cu(OH)2共热
B.将绿豆大小的钠投入到B中,钠块浮在液面上,并产生气泡
C.若C![]() E为加成反应,则D为乙炔
E为加成反应,则D为乙炔
D.为制备干燥的F,可在分离出F后,选用碱石灰做干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】12mL浓度为0.10molL-1的Na2SO3溶液,恰好与10mL浓度为0.04molL-1的K2Cr2O7溶液完全反应,已知Na2SO3能被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为
A. +5
B. +4
C. +3
D. +2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2017长宁区一模】不能用勒夏特列原理解释的是( )
A.使用铁触媒,加快合成氨反应速率
B.过量空气有利于SO2转化为SO3
C.打开汽水瓶盖,即有大量气泡逸出
D.配置FeCl3溶液时,加入少量盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,将1 mL pH=1的H2SO4溶液加水稀释到100 mL,稀释后的溶液中![]() =________。
=________。
(2)某温度时,测得0.01 mol·L-1的NaOH溶液的pH=11,则该温度下水的离子积常数KW=____________,该温度____________25 ℃。(填“>”、“=”或“<”)
(3) 在(2)所述温度下,将pH=12的NaOH溶液Va L与pH=2的硫酸Vb L混合。若所得混合液的pH=10,则Va∶Vb=___________。
(4) 常温下,将1mL pH均为11的氨水与NaOH溶液分别加水稀释,请在答题卷的图中画出两溶液的pH随体积稀释倍数的变化曲线(加必要标注)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用物质的量浓度为0.100 0 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液,选择酚酞作指示剂。请填写下列空白:
(1) 用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,直到因加入一滴盐酸,溶液_________________,立即停止滴定。
(2) 下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填序号)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出

(3) 若某次滴定结束时,酸式滴定管中的液面如图所示,则读数为 mL。若仰视,会使读数偏___________(填“大”或“小”)。
(4) 再结合下表数据,计算被测氢氧化钠溶液的物质的量浓度是 mol·L-1。
滴定 次数 | 待测溶液 体积/mL | 标准酸体积 | |
滴定前的刻度/mL | 滴定后的刻度/mL | ||
第一次 | 10.00 | 1.34 | 19.39 |
第二次 | 10.00 | 4.10 | 21.10 |
第三次 | 10.00 | 0.40 | 17.60 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极分别电解下列各物质的水溶液一段时间后,向剩余溶液中加入适量水能使溶液恢复到电解前浓度的是
A.AgNO3 B.NaCl C.CuCl2 D.H2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com