
【题目】人的胃壁能产生胃液,胃液里含有少量盐酸,称为胃酸。胃过多会导致消化不良和胃痛。抗酸药是一类治疗胃痛的药物,能中和胃里过多的盐酸,缓解胃部的不适。下列物质不能作抗酸药的是( )
A.碳酸氢钠B.氢氧化铝C.碳酸镁D.硫酸钡
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】利用芳香烃X和烯烃Y可以合成紫外线吸收剂BAD.
已知:G不能发生银镜反应,B遇FeCl3溶液显紫色,C到D的过程为引入羧基(﹣COOH)的反应.其中BAD结构简式为: 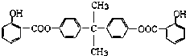
BAD的合成路线如下: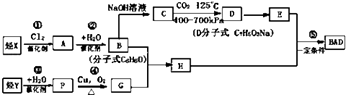
试回答下列问题:
(1)写出结构简式YD .
(2)属于加成反应的有(填数字序号) .
(3)1molBAD最多可与含molNaOH的溶液完全反应.
(4)写出方程式反应④ . F+E .
(5)E有多种同分异构体,判断符合下列要求的同分异构体数目为种.
①能发生银镜反应②遇FeCl3溶液显紫色③核磁共振氢谱图中有四个吸收峰.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生课外活动小组设计了如图所示装置,你认为该装置应选用的试剂是( )

A. I是NaOH溶液 II.是Ca(OH)2溶液
B. I是Ca(OH)2溶液 II.是NaOH溶液
C. I是稀盐酸 II.是Ca(OH)2溶液
D. I是NaOH溶液 II.是CaCl2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.常温下,PH=9的碳酸钠溶液中由水电离出的c(OH﹣)=1×10﹣9molL﹣1
B.饱和氯水中:c(Cl﹣)=c(ClO﹣)+c(HClO)
C.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D.中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NH4NO3溶于水得无色溶液,为使该溶液中的c(NH ![]() ):c(NO
):c(NO ![]() )=1:1,可以采取的下列措施是( )
)=1:1,可以采取的下列措施是( )
A.加入适量的HNO3 , 抑制NH ![]() 水解
水解
B.加入适量的氨水,使溶液的pH等于7
C.再加入适量的NH4NO3(s)
D.加入适量的NaOH,使溶液的pH等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,向密闭恒容容器中加入1.0mol/L X,发生反应:2X(g)Y(g)+Z(g),△H<0,反应到8min时达到平衡;在14min时改变的温度,16min时建立新平衡.X的物质的量浓度变化如图所示.下列有关说法正确的是( ) 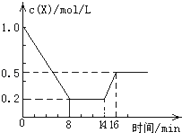
A.0~8min用Y表示的该反应的速度为0.1mol/Lmin
B.8min时达到平衡,该反应的平衡常数为 K=0.5
C.14min时,改变的反应条件是降低了体系的温度
D.16min时的正反应速率,比8min时的正反应速率大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备氮化镁的装置示意图如下: 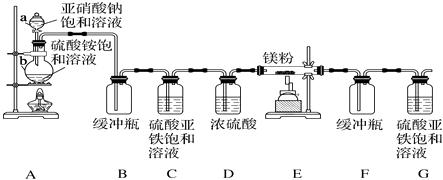
回答下列问题:
(1)仪器a的名称是 , b的名称是 .
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式: .
(3)C的作用是 .
(4)写出E中发生反应的化学方程式: .
(5)请用化学方法确定氮化镁是否含有未反应的镁,写出实验操作及现象 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.52g铜镁合金完全溶解于足量的浓硝酸中,得到NO2气体1344mL (标准状况),向反应后的溶液中加入1.0mol/L NaOH溶液,发现金属离子全部沉淀,下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B.可得到2.54 g沉淀
C.如果是铜铝合金,则产生的NO2 的体积不会是1344mL
D.恰好全部沉淀时,加入NaOH溶液的体积是600 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于原子核外电子排布的下列叙述不正确的是
A.核外电子总是尽可能排布在能量最低的电子层
B.每一个电子层最多可容纳的电子数为2n2
C.某原子的核外最外层最多可容纳8个电子
D.当M层为次外层时,最多可容纳18个电子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com