
【题目】已知N2H4在水中电离方式与NH3相似,若将NH3视为一元弱碱,则N2H4是一种二元弱碱,下列关于N2H4的说法不正确的是
A.它与硫酸形成的酸式盐可以表示为N2H5HSO4
B.它溶于水所得的溶液中共有4种离子
C.它溶于水发生电离的第一步可表示为:N2H4+H2O![]() N2H5+OH-
N2H5+OH-
D.室温下,向0.1mol/L的N2H4溶液加水稀释时,n(H+)·n(OH-)会增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 常温下,将pH=3的醋酸溶液加水稀释到原体积的10倍后,溶液的pH=4
B. 为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C. pH=13的NaOH溶液与pH=1的醋酸溶液等体积混合后所得溶液的pH>7
D. 向氨水中逐滴滴入盐酸至溶液的pH=7,则混合液中:c(NH4+) = c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L的恒容密闭容器中充入2 mol SO2和1 mol O2,发生反应:2SO2(g) + O2(g)![]() 2SO3(g),下列有关说法正确的是( )
2SO3(g),下列有关说法正确的是( )
A.由图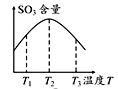 可知:该反应的△H<0
可知:该反应的△H<0
B.在图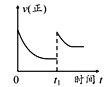 中的t1时充入少量氩气,容器内压强增大,平衡右移
中的t1时充入少量氩气,容器内压强增大,平衡右移
C.图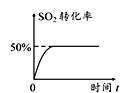 所示条件下,平衡常数为2
所示条件下,平衡常数为2
D.图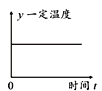 中的y可以表示平衡常数或混合气体平均摩尔质量
中的y可以表示平衡常数或混合气体平均摩尔质量
查看答案和解析>>
科目:高中化学 来源: 题型:
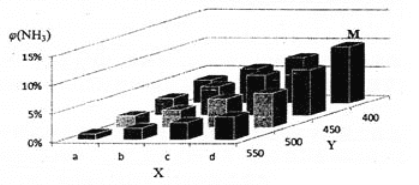
【题目】1913年,德国化学家哈伯实现了合成氨的工业化生产,被称作解救世界粮食危机的化学天才。现将lmolN2和3molH2投入1L的密闭容器,在一定条件下,利用如下反应模拟哈伯合成氨的工业化生产: N2(g) +3H2(g) ![]() 2NH3(g)△H < 0 当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如下图所示。
2NH3(g)△H < 0 当改变某一外界条件(温度或压强)时,NH3的体积分数φ(NH3)变化趋势如下图所示。
(1)已知:①NH3(l) ![]() NH3(g) ΔH1 ②N2(g)+3H2(g)
NH3(g) ΔH1 ②N2(g)+3H2(g) ![]() 2NH3(l) ΔH2,则反应N2(g)+3H2(g)
2NH3(l) ΔH2,则反应N2(g)+3H2(g) ![]() 2NH3(g)的△H=________(用含△H1、△H2的代数式表示)。
2NH3(g)的△H=________(用含△H1、△H2的代数式表示)。
(2)X轴上a点的数值比b点 _____(填“大”或“小”),Y轴表示_______(填“温度”或“压强”)。
(3)将1mol N2和3mol H2分别投入起始容积为1L的密闭容器中,实验条件相关数据如下表所示:
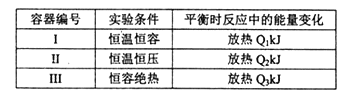
下列判断正确的是________。
A.放出热量:Ql< Q2<|△H| B.N2的转化率:I> III
C.平衡常数:II >I D.达平衡时氨气的体积分数:I>II
(4)平衡时,M点NH3的体积分数为10%。若同温同容下,再充入0.2mol N2,0.6mol H2和1.6molNH 3,重新达平衡时NH3的体积分数________ 10%(填“>”、“<”、“=”或“无法确定”)。
(5)某科研小组探究在其他条件不变的情况下,改变起始物氢气的物质的量对合成NH3反应的影响.实验结果如图所示:(图中T2和T1表示温度,n表示起始时H2的物质的量)
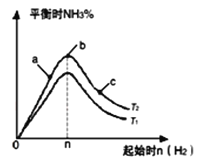
①图象中T2和T1的关系是:T2_____T1(填“>”、“<”、“=”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N2的转化率最大的是___(填字母)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) 2016中国首艘国产航母即将竣工,8艘052D驱逐舰下水,加快了我国海军迈向“蓝水海军”的步伐。

①舰艇底部涂有含Cu2O的防腐蚀涂料。Cu2O属于________(填字母)。
a. 复合材料
b. 无机非金属材料
c. 有机高分子材料
②核动力航母中,钠钾合金(常温下呈液态)可用于快中子反应堆导热剂,是利用了钠钾合金性质的________(填字母)。
a. 熔点低、沸点高 b. 导电性好 c. 在空气中性质不稳定
③航母中供水管道多采用PE(聚乙烯)材料,聚乙烯的化学式为________________。
(2)西兰花营养丰富,含蛋白质、淀粉、油脂、叶酸、维生素C和叶绿素,营养成份位居同类蔬菜之首,被誉为“蔬菜皇冠”。

①维生素C俗名为________。在一支盛有2 mL 2%淀粉溶液的试管中滴入2滴碘 水,溶液呈蓝色,再滴入维生素C的水溶液,溶液颜色变为________,该实验说明维生素C具有________性。
②油脂在人体内水解的最终产物是________(写名称)和甘油。
③西兰花成分中可做天然着色剂的是________,属于糖类的是________。
(3) 2016年9月4日,G20峰会召开,扬州天空呈现出干净的蓝色,云彩随意地铺散在天空,纯净透明,出现了持续的“水晶天”。
①目前我国空气质量检测体系包括:PM2.5、SO2、NO2、O3、CO等指标。其中________被认为是引起雾霾天气的元凶;会引起硫酸型酸雨的气体为________。
②NH3催化还原氮氧化合物转化为无污染物质是目前应用最广泛的烟气氮氧化合物脱除技术,写出NH3催化还原NO2反应的化学方程式________________。
③减少CO2的排放对于环境保护具有重要意义。在海洋碳循环中,可通 过如图所示的途径固碳。写出钙化作用的离子方程式:________________。
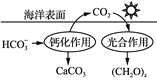
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,在一个密闭的玻璃管两端各放一团棉花,再用注射器同时在两端注入适量的浓氨水和浓盐酸,下列说法不正确的是
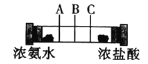
A.玻璃管中发生的反应可表示为:NH3+HCl=NH4Cl
B.实验时会在玻璃管的A处附近看到白雾
C.用手触摸玻璃管外壁,会感觉到有热量放出
D.将浓盐酸换成浓硝酸也会有相似现象
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硫、氮气、二氧化碳组成的混合气体在同温、同压下与笑气(N2O)的密度相同,则该混合气体中二氧化硫、氮气、二氧化碳的质量比为( )
A.4:5:6B.22:1:14
C.64:35:13D.29:8:13
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. NaCl(aq)![]() Cl2(g)
Cl2(g)![]() FeCl2(s)
FeCl2(s)
B. MgCl2(aq)![]() Mg(OH)2(s)
Mg(OH)2(s)![]() MgO (s)
MgO (s)
C. S(s)![]() SO3(g)
SO3(g)![]() H2SO4(aq)
H2SO4(aq)
D. N2(g)![]() NH3(g)
NH3(g)![]() Na2CO3(s)
Na2CO3(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2C2O4是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中H2C2O4、HC2O4-、C2O42-的组成百分率与pH的关系如图所示,下列说法正确的是
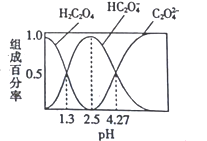
A. pH=4.27的溶液中:c(K+)+c(H+)=c(OH-)+3c(C2O42-)
B. 反应HC2O4-+H2O![]() H2C2O4+OH-的平衡常数为10-4.27
H2C2O4+OH-的平衡常数为10-4.27
C. 向溶液中加入KOH溶液将pH由1.3调至4.27的过程中水的电离程度先增大后减小
D. pH=2.5的溶液中:c(H+)+2c(H2C2O4)=c(OH-)+c(C2O42-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com