
【题目】根据酸碱质子理论判断,下列说法正确的是( )
A.由于水是中性的,故它既不是酸,也不是碱
B.![]() 可以被看作酸碱两性物质,与
可以被看作酸碱两性物质,与![]() 相似,
相似,![]() 也可以被看作酸碱两性物质
也可以被看作酸碱两性物质
C.![]() 溶液显酸性,
溶液显酸性,![]() 只能被看作酸
只能被看作酸
D.不但酸和碱可以用酸碱质子理论来分析,盐和水也可以用酸碱质子理论来分析
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】煤和石油是化工原料的重要来源,从石油中获得A,是工业上生产A的主要途径,A可用作植物生长调节剂。从煤焦油中可获得烃B,B中碳、氢两种元素的质量比为12:1,且B是常见的有机溶剂。工业上可以通过以下途径获得A、B。
![]()
![]()
(1)由煤得到煤焦油的方法称为________;由石蜡油获得A的方法称为________。
(2)A和B中,能使酸性高锰酸钾溶液褪色的是________(填“A”或“B”)。
(3)写出B发生取代反应的化学方程式:________________________(写一个即可,并注明反应条件)。
(4)用B和丙烯可以生产两种重要的化工原料:苯酚(![]() )和丙酮(
)和丙酮(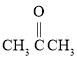 ),生产流程如下:
),生产流程如下:
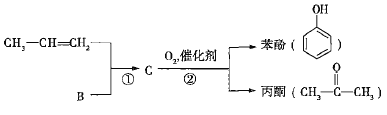
已知反应①是加成反应,C的一氯代物有5种,则C的结构简式为_____________;反应②的化学方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质在适宜的条件下反应,其中氧化剂与还原剂的物质的量之比为2:1的是( )
A. ![]()
B. Fe2O3+2Al![]() Al2O3+2Fe
Al2O3+2Fe
C. CaH2+2H2O===Ca(OH)2+2H2↑
D. 3NO2+H2O===2HNO3+NO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向20.00mL0.1mol·L-1H2X溶液中滴入0.1mol·L-1 NaOH溶液,溶液中由水电离出的c水(OH-)的负对数[-1gc水(OH-)]与所加NaOH溶液体积的关系如图所示。

下列说法中正确的是
A. 水的电离程度:M>N=Q>P
B. 图中M、P、Q三点对应溶液中![]() 相等
相等
C. N点溶液中c(Na+)>c(X2-)>c(HX-)>c(H+)=c(OH-)
D. P点溶液中c(OH-)=c(H+)+c(HX-)+c(H2X)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组用下列装置进行乙醇催化氧化的实验。

(1)请写出装有铜网的试管中反应的化学方程式:___。
(2)不断鼓入空气,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化氧化反应是____反应(填“吸热”或“放热”)。
(3)甲和乙两个水浴作用不相同。甲的作用是___;乙的作用是___。
(4)反应进行一段时间后,集气瓶收集到的气体主要是___。
(5)若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,要除去该物质,选择的试剂是__(填写字母):
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.金属钠
再通过___(填实验操作名称)即可得到乙醛。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以淀粉和油脂为原料,制备生活中某些物质。
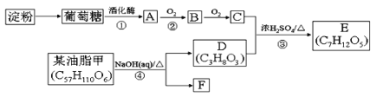
请回答下列问题:
(1)淀粉的分子式为____。
(2)③的反应类型___。
(3)写出反应①的化学方程式:____。写出反应④的化学方程式:____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项正确的是![]()
A.使PH试纸变成红色的溶液,可能存在大量的:![]() 、
、![]() 、
、![]() 、
、![]()
B.![]() 溶液中,可能存在大量的:
溶液中,可能存在大量的:![]() 、
、![]() 、
、![]() 、
、![]()
C.硫酸酸化的淀粉KI溶液在空气中变成蓝色:![]()
D.![]() 溶液中滴加少量澄清石灰水:
溶液中滴加少量澄清石灰水:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢能被视为21世纪最具发展潜力的清洁能源。
(1)水是制取H2的常见原料,下列有关水的说法正确的是______.
a.水分子是一种极性分子,水分子空间结构呈直线型
b.1个H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H﹣O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键。
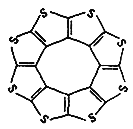
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为______,C16S8中σ键与π键之比为______,C16S8与H2微粒间的作用力是______。
②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(用“→”表示)的氨硼烷的结构式_____;与氨硼烷互为等电子体的有机小分子是___(写结构简式)。
③某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进人到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(晶胞结构如图)的结构相似,该晶体储氢后Cu:Au:H为______。
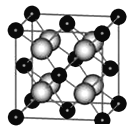
④MgH2是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度ag·cm-3,则晶胞的体积为______________cm3(用含a、NA的代数式表示,NA表示阿伏伽德罗常数)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,物质之间通过一步反应就能实现如图所示转化的是( )
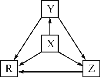
选项 | X | Y | Z | R |
A | Al | AlCl3 | Al(OH)3 | NaAlO2 |
B | Na | Na2O | Na2O2 | NaOH |
C | H2S | S | SO2 | SO3 |
D | N2 | NH3 | NO | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com