
【题目】利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组在实验室中模拟上述过程,其设计的模拟装置如下:
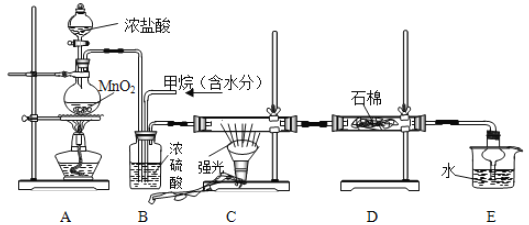
试回答下列问题:
(1)请写出C装置中生成CH3Cl的化学反应方程式:___________。
(2)B装置有三种功能;①控制气流速度;②混匀混合气体;③________。
(3)一段时间后发现D装置中的棉花由白色变为蓝色,则棉花上可能预先滴有___溶液。
(4)E装置中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为________(填字母)。
A分液法 B蒸馏法 C结晶法
(5)将1molCH4与Cl2发生取代反应,充分反应后生成的CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为_____,生成HCl的物质的量共为________。
【答案】CH4 + Cl2![]() CH3Cl + HCl 干燥氯气 淀粉KI溶液 A 3mol 3mol
CH3Cl + HCl 干燥氯气 淀粉KI溶液 A 3mol 3mol
【解析】
紧扣主体反应:甲烷与氯气的光照取代反应,从原料的制备与混合、剩余反应物的检验、产物的分离入手,分析解答问题。主体反应是连续进行的四步取代反应,应用化学方程式计算参加反应的Cl2的物质的量和生成HCl的物质的量。
(1)装置C中,甲烷与氯气在光照条件下发生取代反应,其中生成CH3Cl的化学方程式为
CH4 + Cl2![]() CH3Cl + HCl。
CH3Cl + HCl。
(2)装置B中盛有浓硫酸,氯气、甲烷通过后进入装置C。可见装置B有三种功能:①控制气流速度;②混匀混合气体;③干燥氯气、甲烷。
(3)进入装置D的物质为甲烷的氯代物、氯化氢,以及未反应的甲烷、氯气,其中氯气能使湿润的淀粉碘化钾溶液变蓝。装置D中的棉花可能预先滴有淀粉碘化钾溶液。
(4)甲烷的氯代产物中,四种氯代物均不溶于水、只有氯化氢溶于水成盐酸。从装置E中分离出盐酸的最佳方法为分液法。
(5)设CH3Cl的物质的量为x,则CH2Cl2、CHCl3、CCl4的物质的量分别为x+0.1mol、x+0.2mol、x+0.3mol。则x+(x+0.1mol)+(x+0.2mol)+(x+0.3mol)=1 mol,解得x=0.1mol。
①CH4+Cl2![]() CH3Cl+HCl,生成0.1molCH3Cl,消耗0.1molCl2、生成0.1molHCl。
CH3Cl+HCl,生成0.1molCH3Cl,消耗0.1molCl2、生成0.1molHCl。
②CH4+2Cl2![]() CH2Cl2+2HCl,生成0.2molCH2Cl2,消耗0.4molCl2、生成0.4molHCl。
CH2Cl2+2HCl,生成0.2molCH2Cl2,消耗0.4molCl2、生成0.4molHCl。
③CH4+3Cl2![]() CHCl3+3HCl,生成0.3molCHCl3,消耗0.9molCl2、生成0.9molHCl。
CHCl3+3HCl,生成0.3molCHCl3,消耗0.9molCl2、生成0.9molHCl。
④CH4+4Cl2![]() CCl4+4HCl,生成0.4molCCl4,消耗1.6molCl2、生成1.6molHCl。
CCl4+4HCl,生成0.4molCCl4,消耗1.6molCl2、生成1.6molHCl。
共消耗3molCl2,生成3molHCl。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】在2L的密闭容器中发生反应:4A(s)+3B(g)2C(g)+D(g),2min后B减小了1.2mol.有关此反应的说法正确的是( )
A. 在 2min 内的反应速率,用 C 表示是 0.4mol/(Lmin)
B. 分别用 B、C、D 表示化学反应速率其比值是 3:2:1
C. 达到化学反应限度时,B 物质转化率为 100%
D. 向容器中增加 A 的投量,可以加快该反应的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SiCl4在室温下为无色液体,易挥发,有强烈的刺激性。把SiCl4先转化为SiHCl3,再经氢气还原生成高纯硅。一定条件下,在20L恒容密闭容器中发生SiCl4转化为SiHCl3的反应:3SiCl4(g)+2H2(g)+Si(s)SiHCl3(g),△H=QkJmol-1,2min后达到平衡,H2与SiHCl3的物质的量浓度分别为0.1mol/L和0.2mol/L。
(1)从反应开始到平衡,v(SiCl4)=_______
(2)该反应的平衡常数表达式为K=_______,温度升高,K值增大,则Q__0(填“>”、“<”或“=”)。
(3)若平衡后再向容器中充入与起始时等量的SiCl4和H2(假设Si足量),当反应再次达到平衡时,与原平衡相比较,H2的体积分数将____(填“增大”、“减小”或“不变”)。
(4)原容器中,通入H2的体积(标准状况下)为_________
(5)平衡后,将容器的体积缩为10L,再次达到平衡时,H2的物质的量浓度范围为__________
(6)图中x轴表示温度,y轴表示平衡混合气中H2的体积分数,a、b表示不同的压强,则压强a____b(填“>”、“<”或“=”)。
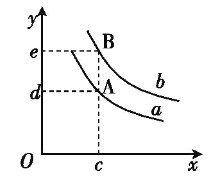
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于![]() (I)、
(I)、![]() (II)、
(II)、![]() (III)、
(III)、![]() (IV)化合物的说法正确的是
(IV)化合物的说法正确的是
A. Ⅰ、Ⅱ、Ⅲ、Ⅳ的沸点依次升高 B. Ⅰ、Ⅲ的一氯代物均只有四种
C. Ⅱ、Ⅲ中碳原子可能都处于同一平面 D. Ⅲ、Ⅳ都属于芳香族化合物,互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6.54g氧化铜与石墨的混合粉末隔绝空气加热,充分反应后,生成的气体用足量的NaOH溶液吸收,溶液增重1.32g。则原混合粉末中氧化铜的质量可能是
A.2.4gB.4.8gC.6gD.6.18g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。
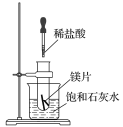
回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)写出有关反应的离子方程式____________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A可以通过不同化学反应分别制得B、C和D三种物质,结构简式如图所示:
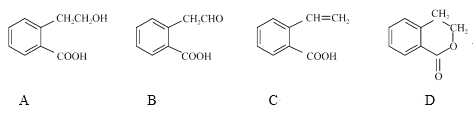
(1)A的分子式是____;B中的含氧官能团名称是____。
(2)A→B的反应类型是___;A~D中互为同分异构体的是___(填代号)。
(3)D在酸性条件下水解的化学方程式是____。
(4)B与足量新制Cu(OH)2悬浊液反应的化学方程式是___________。
(5)符合下列条件的A的同分异构体有____种。
①官能团与A完全相同且与苯环直接相连;②苯环上有三个取代基。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,还含有少量Fe2+、Fe3+和Mn2+等杂质离子。现以卤块为原料按如下流程进行生产,以制备金属镁。

本流程操作条件下,生成氢氧化物沉淀的pH如下表:
物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
开始沉淀 | 2.7 | 7.6 | 8.3 | 10.0 |
沉淀完全 | 3.7 | 9.6 | 9.8 | 11.1 |
*Fe2+氧氧化物呈絮状,不易从溶液中除去,常将它氧化为Fe3+后生成Fe(OH)3沉淀除去。 请回答以下问题:
(1)步骤①中,为了加快酸溶速率,除了适当增加稀盐酸的浓度外,还可以采取的措施有 __________________________ (任写一条)。
(2)步骤②中NaClO的电子式为__________,加入NaClO溶液的目的是_________________________
(用离子方程式解释)。
(3)常温时,Mg(OH)2的Ksp=1.8×10-11。当溶液pH=10.0时,溶液中的c(Mg2+)=___________。
(4)若将步骤⑤中“稀盐酸”改为“加水、煮沸”的方式可以得到另一种沉淀物和一种无色无味的气体,请写出该反应的化学方程式__________________________________________。
(5)步骤⑥中涉及的操作是_____________________________,且⑥⑦操作均需在HCl气流中进行,其原因是_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com