
【题目】关于次氯酸的叙述错误的是( )
A.属于强酸B.弱电解质C.不稳定D.有氧化性
科目:高中化学 来源: 题型:
【题目】(14分)Fe是人体不可缺少的微量元素,摄入含铁化合物可补充铁。硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定某补血剂中铁元素的含量。实验步骤如下:

请回答下列问题:
(1)步骤②中加入足量NaOH发生的主要反应的离子方程式为 ,
步骤③中反应的化学方程式为 。
(2)步骤④中一系列处理的操作步骤: 、洗涤、 、冷却、称量。
(3)若实验中需用98%的浓硫酸(密度为1.84g/mL)配制1 mol/L的稀硫酸480 mL。配制时用到的玻璃仪器除量筒、烧杯、胶头滴管、玻璃棒外还有 ,需用量筒量取该浓硫酸 mL。
(4)若实验无损耗,则每片补血剂含铁元素的质量 g(用含a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学探究的基本程序包括形成问题、建立假设、设计研究方案、检验假设、表达或交流结果等.某同学欲用如图装置可用来探究浓硫酸与木炭粉的加热条件下反应产生的所有气体产物,请填写下列空白:

(1)写出木炭粉与浓硫酸反应的化学方程式____________
(2)②中品红溶液A的作用是 ______ .酸性高锰酸钾的作用______品红溶液B的作用是______。
(3)如果将装置中①、②、③三部分仪器的连接顺序改为②、①、③:则可以检出的物质是_____,不能检出的物质是_____ 。
(4)如果将仪器的连接顺序变为①、③、②,则不能检出的物质是 ______。
(5)如果将仪器的连接顺序变为②、③、①,则不能检出的物质是 ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,科学家新研制的一种酸性乙醇电池(用磺酸类质子作溶剂),比甲醇电池效率高出32倍,电池反应式为C2H5OH+3O2=== 2CO2+3H2O,电池构造如下图所示:
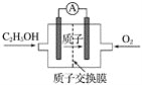
下列关于该电池的说法不正确的是( )
A. 通入乙醇的一极为负极
B. 正极反应式为4H++O2+4e-===2H2O
C. 负极反应式为C2H5OH-12e-+3H2O===2CO2+12H+
D. 随着反应的进行,溶液的酸性保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制乙烯时,产生的气体能使溴水褪色,甲、乙同学用下列实验验证。
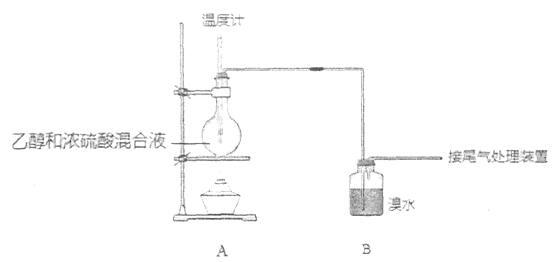
(气密性已检验,部分夹持装置略)。实验操作和现象为:
操作 | 现象 |
点燃酒精灯,加热至170℃ | I:A中烧瓶内液体渐渐变黑 II:B内气泡连续冒出,溶液逐渐褪色 |
…… | |
实验完毕,清洗烧瓶 | III:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(1)烧瓶内产生乙烯的化学方程式是________。
(2)溶液“渐渐变黑”,说明浓硫酸具有________性。
(3)分析使B中溶液褪色的物质,甲认为是C2H4,乙认为不能排除SO2的作用。
①根据甲的观点,使B中溶液褪色反应的化学方程式是________。
②乙根据现象III认为产生了SO2,在B中与SO2反应使溶液褪色的物质是________。
③为证实各自观点,甲、乙重新实验,设计与现象如下:
设计 | 现象 | |
甲 | 在A、B间增加一个装有某种试剂的洗气瓶 | 溴水褪色 |
乙 | 与A连接的装置如下:
| D中溶液由红棕色变为浅红棕色时,E中溶液褪色 |
a. 根据甲的设计,洗气瓶中盛放的试剂是________。
b. 根据乙的设计,C中盛放的试剂是________。
c. 能证明确实是SO2使E中溶液褪色的实验是________。
d. 乙为进一步验证其观点,取少量D中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是________。
(4)上述实验得到的结论是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组研究铝土矿中Al2O3的含量。已知铝土矿的主要成分是Al2O3,杂质是Fe2O3、SiO2等。从铝土矿中提取Al2O3的过程如下:

(1)流程甲中加入盐酸后生成Fe3+的离子方程式为____________;固体A_____(填化学式),写出沉淀F转化为氧化铝的化学方程式是_______________。
(2)流程乙中向铝土矿中加入过量烧碱溶液后,发生反应的离子方程式是______、________;沉淀Z为_______(填化学式)。由溶液K生成沉淀M的离子方程式是__________。
(3)流程乙中将实验过程中所得固体精确称量,课外小组发现所得氢氧化铝固体的质量与原铝土矿质量相等,则该铝土矿中Al2O3的质量分数是________(保留一位小数)。
(4)工业上制取AlCl3:用Al2O3与C、Cl2在高温条件下反应,每消耗0.5mol碳单质,转移1mol电子,反应的化学方程式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】地壳中含量位于第一、二位的元素之间形成的化合物不具有的性质是( )
A.常温下能与苛性钠反应B.常温下能与水反应
C.常温下能与氢氟酸反应D.高温时能与氧化钙反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于明矾可以净水的原因,下列叙述正确的是( )
A.明矾中的硫酸根离子与水中的阳离子结合生成沉淀
B.明矾中的金属铝离子能生成氢氧化铝沉淀
C.明矾溶于水后,生成氢氧化铝胶体,起到净水作用
D.明矾溶于水后,电离产生的金属阳离子吸附能力强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com