
【题目】在25℃时,用蒸馏水稀释1mol·L-1的氨水至0.01mol·L-1,随着溶液的稀释,下列各项比值中始终不变的是( )
A.![]() B.
B.![]()
C.![]() D.
D.![]()
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】甘氨酸亚铁络合物[(H2NCH2COO)2Fe]是一种新型的铁营养强化剂,广泛用于缺铁性贫血的预防和治疗。某学习小组模拟其合成方法,如图:
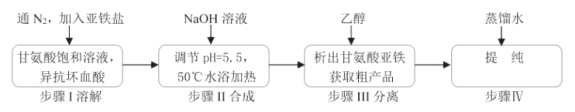
已知:

请回答:
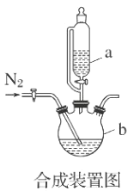
(1)合成装置中仪器a中玻璃导管的作用是__。
(2)合成过程中,本实验为了防止Fe2+被氧化,采取的措施有__,__。
(3)写出水浴加热过程中生成甘氨酸亚铁络合物的离子方程式___。
(4)下列说法正确的是__。
A.滴入液体前,应先打开滴液漏斗a的上口玻璃塞
B.根据题中所给信息,亚铁盐应选用FeSO4·7H2O
C.步骤Ⅲ中的分离方法是过滤
D.步骤IV,提纯操作中的干燥过程最好选用真空干燥
(5)合成过程需控制pH=5.5,试说明理由___。
(6)步骤Ⅲ加入无水乙醇的目的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓硫酸,浓硫酸增重30.6 g ,然后通过碱石灰,碱石灰增重52.8 g,混合气体中乙烷和丙烷的体积比为( )
A.1∶1
B.2∶3
C.3∶2
D.3∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】800℃时,在2 L密闭容器中发生反应:2NO(g)+O2(g)![]() 2NO2(g),该反应体系中n(NO)随时间的变化如下表:
2NO2(g),该反应体系中n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.022 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
下列有关说法不正确的是
A. 用氧气表示0~3 s内该反应的平均速率ν(O2)=0.0025 mol·L-1·s-1
B. 容器内颜色保持不变时,说明该反应达到平衡状态
C. 增大氧气的浓度,既加快反应速率,又使平衡正向移动
D. 该反应达到平衡时,转移电子总数为0.03NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.常温下,pH=7的溶液不一定是纯水
B.常温下,某氨水pH=x,某盐酸pH=14-x,两者等体积混合后,pH>7
C.相同温度下,pH相等的盐酸、CH3COOH溶液中,c(CH3COO-)= c(Cl-)
D.氨水和硫酸反应后的溶液,若溶液呈中性,则c(![]() )=c(
)=c(![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①N2(g)+2O2(g)![]() 2NO2(g) △H=+67.7kJ/mol
2NO2(g) △H=+67.7kJ/mol
②2N2H4(g)+2O2(g)![]() 2N2(g)+4H2O(g) △H=-1068kJ/mol
2N2(g)+4H2O(g) △H=-1068kJ/mol
(1)火箭发射时可用肼(N2H4)作燃料,以二氧化氮作氧化剂,它们相互反应生成氮气和水蒸气。根据盖斯定律写出N2H 4和NO2反应的热化学方程式为____;
(2)肼(N2H4)和氧气反应的能量变化如图所示,图中E1表示___,E2表示____,△H=-534kJ/mol表示_____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下将8.96 L氯化氢气体溶于水形成100 mL溶液,然后与足量的铁屑反应。
(1)所得盐酸溶液的物质的量浓度是多少________?
(2)参加反应的铁的质量是多少________?
(3)标况下生成氢气的体积是多少________?
(4)将生成的氯化亚铁配成400 mL溶液,此溶液中氯化亚铁的物质的量浓度是多少________?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学就在我们身边,它与我们的日常生活密切相关,按要求回答以下问题:
(1)缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是_________________.
(2)硅酸盐常可写成氧化物形式,钾长石(K2Al2Si6O16)写成氧化物的形式为____________.
(3)漂粉精中有效成分的化学式为_________________.
(4)“硅材料”是无机非金属材料的主角,其中广泛应用的光导纤维成分是_____________________
(5)陶瓷、水泥和玻璃是常用的传统的无机非金属材料,其中生产普通玻璃的主要原料有_________,氢氧化钠溶液不能用玻璃塞的原因是(化学方程式)_________________.
(6)向浑浊的水中加入明矾KAl(SO4)212H2O后,水可得到净化.写出明矾在水中的电离方程式_______,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为_________________ .
(7)饮用水中的NO3-对人类健康产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.
请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:_________________.
②上述反应中若生成标况下3.36L N2,则转移的电子数目为:_________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应的能量变化示意图如下,有关说法正确的是( )
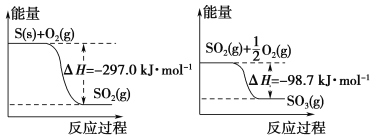
A. 1 mol S(g)与O2(g)完全反应生成SO2(g),反应放出的热量小于297.0 kJ
B. 在相同条件下,SO2(g)比SO3(g)稳定
C. S(s)与O2(g)反应生成SO3(g)的热化学方程式S(s)+![]() O2(g)
O2(g)![]() SO3(g) ΔH=+395.7 kJ·mol-1
SO3(g) ΔH=+395.7 kJ·mol-1
D. 一定条件下1 mol SO2(g)和![]() mol O2(g)反应,生成1 mol SO3(l)放出热量大于98.7 kJ
mol O2(g)反应,生成1 mol SO3(l)放出热量大于98.7 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com