
【题目】一氯甲烷(CH3Cl)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
(1)甲组同学在实验室用下图所示装置模拟催化法制备和收集一氯甲烷。

①仪器a的名称为___________。
②无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为_____________。
③装置B的主要作用是_____________。
(2)乙组同学选用甲组A、B装置和下图所示的部分装置检验CH3Cl中的氯元素。

①乙组同学的实验装置中,依次连接的合理顺序为A→B→_____→_____→_____。
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞先后加入两种试剂,观察实验现象。分液漏斗中先后加入的试剂是_______________。
③能证明CH3Cl中含有氯元素的实验现象是____________。
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3Cl中的卤素原子。相关数据如下表:

将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中数据解释原因__________________。
【答案】 圆底烧瓶 CH3OH+HCl(浓) ![]() CH3Cl+H2O 除去CH3OH蒸气、HCl等杂质气体 F D G 硝酸、硝酸银 C-Br键的键能小,更容易断裂 Ksp(AgBr)< Ksp(AgCl),AgBr更容易沉淀
CH3Cl+H2O 除去CH3OH蒸气、HCl等杂质气体 F D G 硝酸、硝酸银 C-Br键的键能小,更容易断裂 Ksp(AgBr)< Ksp(AgCl),AgBr更容易沉淀
【解析】(1)①根据仪器构造可知仪器a的名称为圆底烧瓶;②甲醇与浓盐酸在作催化剂的条件下发生取代反应生成一氯甲烷和水,反应的化学方程式为CH3OH+HCl(浓) ![]() CH3Cl+H2O;③氯化氢、甲醇均易挥发,所以要用水除去一氯甲烷中的氯化氢和甲醇蒸汽,所以装置B的主要作用是除去氯化氢气体和甲醇;(2)根据题意,检验CH3Cl中的氯元素,可以将一氯甲烷通入到热的氢氧化钠溶液中,反应一段时间后再加入用硝酸酸化的硝酸银溶液,根据是否有白色沉淀生成可判断氯元素的存在,①根据上面的分析可知,装置依次连接的合理顺序为A、B、F、D、G;②根据上面的分析可知,分液漏斗中盛放的试剂是硝酸、硝酸银,故答案为:硝酸、硝酸银;③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成;(3)依据表中数据可知,C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀,所以先出现淡黄色溴化银沉淀。
CH3Cl+H2O;③氯化氢、甲醇均易挥发,所以要用水除去一氯甲烷中的氯化氢和甲醇蒸汽,所以装置B的主要作用是除去氯化氢气体和甲醇;(2)根据题意,检验CH3Cl中的氯元素,可以将一氯甲烷通入到热的氢氧化钠溶液中,反应一段时间后再加入用硝酸酸化的硝酸银溶液,根据是否有白色沉淀生成可判断氯元素的存在,①根据上面的分析可知,装置依次连接的合理顺序为A、B、F、D、G;②根据上面的分析可知,分液漏斗中盛放的试剂是硝酸、硝酸银,故答案为:硝酸、硝酸银;③能证明CH3Cl中含有氯元素的实验现象是F中无白色沉淀生成,D中有白色沉淀生成;(3)依据表中数据可知,C-Br键的键能小,更容易断裂,同时溴化银的溶度积常数更小,溴化银更容易形成沉淀,所以先出现淡黄色溴化银沉淀。


科目:高中化学 来源: 题型:
【题目】电解质溶液电导率越大导电能力越强。常温下用0.100 mol·L-1盐酸分别滴定10.00 mL浓度均为0.100 mol·L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温Ksp[(CH3)2NH)]=l.6×10-4)。利用传感器测得滴定过程中溶液的电导率如图所示。下列说法正确的是
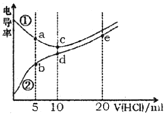
A. 曲线①代表滴定二甲胺溶液的曲线
B. a点溶液中:c[(CH3)2NH2+]>c[CH3]2NH·H2O]
C. d点溶液中:c(H+)=c(OH-)+c[CH3]2NH·H2O]
D. b、c、e三点的溶液中,水的电离程度最大的是b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.地球上99%溴蕴藏在大海中,故溴被称为“海洋元素”
B.高压钠灯发出的黄光射程特别远,故常用于道路与广场的照明
C.碳酸氢钠可与盐酸反应,故可作治疗胃酸过多的药剂
D.利用光线在硅晶体内的全反射现象,可以制备光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol/LNaOH溶液滴定20.00mL 0.10mol/LHA溶液(滴定曲线见图)。下列说法正确的是

A. 此图可以表示从NaOH滴定盐酸的曲线
B. 图中D点状态时溶液中有:c(Na+)<c(A-)
C. 达到D、E状态时,均有:c(Na+)+c(H+)=c(A-)+c(OH-)
D. 当O<V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)> c(Na+)> c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用相同浓度的NaOH溶液,分别滴定100mL浓度均为O.1mol/L的三种酸(HM、HN和HR)溶液,滴定的曲线如图所示,下列判断错误的是

A. 三种酸的电离常数关系:KHM>KHN>KHR
B. pH=7时,三种溶液中:c(M-)>c(N-)>c(R-)
C. 当中和百分数达100%时,将三种溶液混合后:c(HM)+c(HN)+c(HR)=c(OH-)-c(H+)
D. 滴定至P点时,溶液中:c(HN)>c(N-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为短周期主族元素,且原子序数依次增大。A原子的最外层电子数是其电子层数的3倍,B原子的半径在同周期主族元素的原子中最大,A、E同主族,D原子的最高正价与负价的绝对值相等。下列说法正确的是
A. 原子半径:D>CB. 氢化物的稳定性:E>A
C. 氢氧化物的碱性:C>BD. 最高价氧化物对应水化物的酸性:E>D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】航天飞机用铝粉与高氯酸铵(NH4ClO4)的混合物作为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,其方程式可表示为2NH4ClO4 ![]() N2↑+4H2O+Cl2↑+2O2↑,下列对此反应的叙述,错误的是( )
N2↑+4H2O+Cl2↑+2O2↑,下列对此反应的叙述,错误的是( )
A. 此反应属于分解反应
B. 此反应中高氯酸铵只起氧化剂作用
C. 上述反应瞬间产生大量高温气体推动航天飞机飞行
D. 此反应从能量变化上说,主要是化学能转化为热能和动能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.氨气具有还原性,可用作制冷剂
B.氢氟酸具有弱酸性,可用于蚀刻玻璃
C.浓硫酸具有脱水性,可用于干燥CO2
D.二氧化氯具有强氧化性,可用来漂白织物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收尾气中的SO2,将所得的Na2SO3溶液进行电解再生循环脱硫,其原理如图,a、b离子交换膜将电解槽分成为三个区域,电极材料均为石墨。甲~戊分别代表生产中的原料或产品,其中丙为硫酸溶液。下列说法错误的是

A. 图中a表示阳离子交换膜
B. 当电路中通过1mol电子的电量时,会有0.25mol的O2生成
C. 甲为NaOH溶液
D. 阳极的电极反应式为SO32-+H2O-2e-=SO42-+2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com