
| A.两者均表示了物质的变化 |
| B.两者均表示了能量的变化 |
| C.两者均需注明物质的聚集状态及反应条件 |
| D.两者的化学计量数均表示分子数,均必须是整数 |


科目:高中化学 来源:不详 题型:单选题
| A.反应条件是加热的反应都是吸热反应 |
| B.化学反应除了生成新的物质外,还伴随着能量的变化 |
| C.物质燃烧不一定是放热反应 |
| D.放热反应都不需要加热就能发生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.任何化学反应不一定都有反应热 |
| B.能源是提供能量的资源,它包括化石燃料(煤、石油、天然气),不包括阳光、流水 |
| C.对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
| D.在一个确定的化学反应关系中,反应物的总能量总高于生成物的总能量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
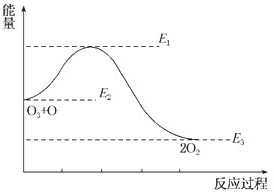
| A.反应O3+O═2O2的△H=E1-E2 |
| B.反应O3+O═2O2的△H=E2-E3 |
| C.反应O3+O═2O2是吸热反应 |
| D.反应O3+O═2O2的△H=△H1+△H2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熵增加且放热的反应一定是自发反应 |
| B.自发反应一定是熵增大的反应,非自发反应一定是熵减小或不变的反应 |
| C.凡是放热反应都是能自发进行的反应,而吸热反应都是非自发进行的反应 |
| D.非自发反应在任何条件下都不能发生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.CO(g)+
| ||
| B.2CO(g)+O2(g)=2CO2(g);△H=-565.9kJ/mol | ||
C.CO(g)+
| ||
D.CO(g)+
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 化学式 | CO(g) | H2(g) | CH3OH(l) |
| △H/(kJ?mol-1) | -283.0 | -285.8 | -726.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该反应的△S<0 |
| B.该反应在任何温度下均能自发进行 |
| C.向容器中充入少量He,平衡向正反应方向移动 |
| D.升高温度平衡向正反应方向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com