
科学家利用淡水与海水之间含盐量的差别发明了一种新型电池——水电池。
(1)用二氧化锰纳米棒作电池正极可提高发电效率,这是利用纳米材料的 特性,使之能与钠离子充分接触。
(2)水电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,该电池的负极反应式为 。水电池工作时,Na+不断向 极方向移动。
(3)水电池生成1 mol Na2Mn5O10转移电子的物质的量为 。
(4)某温度下,Fe(OH)3(s)、Mg(OH)2(s)分别在溶液中达到沉淀溶解平衡后,溶液中金属阳离子的浓度与溶液pH的关系如右图。请据右图分析: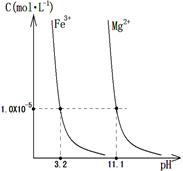
①该温度下,溶度积常数的关系为:KSP[Fe(OH)3] KSP[Mg(OH)2](填“>”、“=”或“<”);
②如果在新生成的Mg(OH)2浊液中滴入足量的FeCl3溶液,振荡后,白色沉淀会全部转化为红褐色沉淀,原因是 。
(1)较强的吸附能力或较大的表面积 (2分)
(2)Ag + Cl--e-=AgCl (3分,2倍计量数、加“↓”不扣分,产物写Ag+不给分) 正(2分)
(3)2 mol(3分,单位错漏扣1分) (4)① < (2分)
②Mg(OH)2浊液中存在沉淀溶解平衡(1分),Mg(OH)2(s)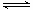 Mg2+(aq)+2OH-(aq),滴入足量的FeCl3溶液,c(Fe3+)×c3(OH―)>KSP[Fe(OH)3],Fe3+与OH-生成更难溶的Fe(OH)3(1分),使Mg(OH)2浊液沉淀溶解平衡向右移动(1分),Mg(OH)2浊液转化为Fe(OH)3沉淀(1分)。(注意要点,合理即给分)
Mg2+(aq)+2OH-(aq),滴入足量的FeCl3溶液,c(Fe3+)×c3(OH―)>KSP[Fe(OH)3],Fe3+与OH-生成更难溶的Fe(OH)3(1分),使Mg(OH)2浊液沉淀溶解平衡向右移动(1分),Mg(OH)2浊液转化为Fe(OH)3沉淀(1分)。(注意要点,合理即给分)
解析试题分析:(1)由于纳米材料的表面积大,具有很强的吸附能力,所以使之能与钠离子充分接触而提高发电效率。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据总反应式5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl可知,Mn元素的化合价从+4价降低到+3.6价,得到电子做氧化剂。Ag元素的化合价从0价升高到+1价失去电子做还原剂。所以银是负极,电极反应式为Ag + Cl--e-=AgCl。水电池工作时,阳离子Na+不断向正极方向移动。
(3)Mn元素的化合价从+4价降低到+3.6价,所以水电池生成1 mol Na2Mn5O10转移电子的物质的量为1mol×5×(4-3.6)=2mol。
(4)①根据图像可知,在金属阳离子的物质的量浓度相同的情况下,氢氧化铁对应的pH小于氢氧化镁对应的pH值,所以氢氧化铁的溶度积常数小于氢氧化镁的溶度积常数。
②由于Mg(OH)2浊液中存在沉淀溶解平衡Mg(OH)2(s)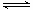 Mg2+(aq)+2OH-(aq),滴入足量的FeCl3溶液,当溶液中c(Fe3+)×c3(OH―)>KSP[Fe(OH)3]时,Fe3+与OH-生成更难溶的Fe(OH)3,使Mg(OH)2浊液的沉淀溶解平衡向右移动,从而使Mg(OH)2浊液全部转化为Fe(OH)3沉淀。
Mg2+(aq)+2OH-(aq),滴入足量的FeCl3溶液,当溶液中c(Fe3+)×c3(OH―)>KSP[Fe(OH)3]时,Fe3+与OH-生成更难溶的Fe(OH)3,使Mg(OH)2浊液的沉淀溶解平衡向右移动,从而使Mg(OH)2浊液全部转化为Fe(OH)3沉淀。
考点:考查纳米材料的性质、电化学原理的应用与判断以及溶度积常数的有关判断与应用


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:填空题
25 ℃时,有关物质的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平 衡常数 | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K=3.0×10-8 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品。
已知:离子沉淀的pH见下表。
| 离子 | 开始沉淀pH | 沉淀完全pH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)有下列物质 ①Cu;②液态SO2;③CH3COOH;④NaHCO3;⑤H2O;⑥熔融NaCl;⑦BaSO4 属于弱电解质的是 (填序号)
(2)常温下,0.1 mol·L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3―、CO32―、OH―四种微粒的浓度由大到小的顺序为: 。NaHCO3水解的离子方程式 。
(3)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液 的pH |
| a | 0.1 | 0.1 | pH=9 |
| b | c | 0.2 | pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某二元酸(化学式用H2A表示)在水溶液中的电离方程式是:
H2A=H++HA-,HA- H++A2-。
H++A2-。
试回答下列问题:
(1)Na2A溶液显________(填“酸性”、“中性”或“碱性”),理由是_____________________(用离子方程式表示)。
(2)若0.1 mol·L-1 NaHA溶液的pH=2,则0.1 mol·L-1 H2A溶液中H+的物质的量浓度________0.11 mol·L-1。(填“>”、“=”或“<”)
(3)0.1 mol·L-1 NaHA溶液中各种离子浓度由大到小的顺序是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某化工厂的含镍废催化剂主要含Ni,还含有Al、Al2O3、Fe、FeO、Fe2O3及其他不溶杂质(其他不溶杂质不与酸碱反应)。某校化学研究性学习小组设计了如下图所示的方法,以该含镍废催化剂为原料来制备NiSO4·7H2O。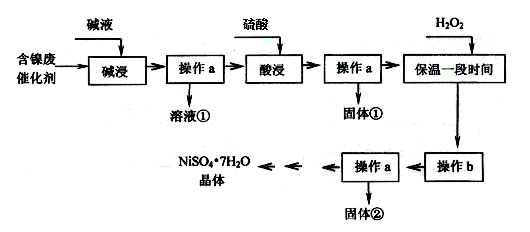
【查阅资料】
①Ni能与非氧化性酸反应生成Ni2+,不与碱液反应。
②部分阳离子以氢氧化物形式沉淀时pH如下:
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 4.1 | 1.7 | 7.6 | 7.0 |
| 完全沉淀的pH | 5.2 | 3.2 | 9.5 | 9.2 |
 2Ni(OH)2,写出该反应放电时正极反应式 。
2Ni(OH)2,写出该反应放电时正极反应式 。 。
。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
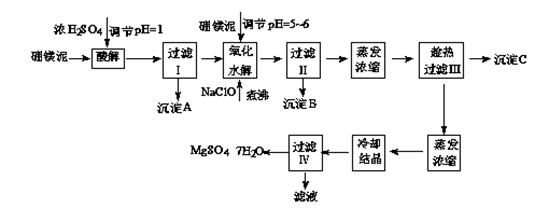
七水硫酸镁(MgSO4·7H2O)在印染、造纸和医药等工业上都有广泛的应用,利用化工厂生产硼砂的废渣-硼镁泥可制取七水硫酸镁。硼镁泥的主要成分是MgCO3,还含有其他杂质(MgO、SiO2、Fe2O3、FeO、CaO、Al2O3、MnO等)。
表1 部分阳离子以氢氧化物形式完全沉淀时溶液的pH
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Mg(OH)2 |
| pH值 | 5.2 | 3.2 | 9.7 | 10.4 | 11.2 |
| 温度/℃ | 10 | 30 | 40 | 50 | 60 |
| CaSO4 | 0.19 | 0.21 | 0.21 | 0.20 | 0.19 |
| MgSO4·7H2O | 30.9 | 35.5 | 40.8 | 45.6 | / |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5的流程如下: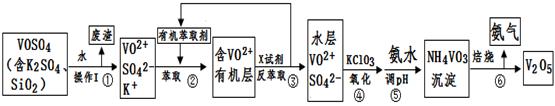
请回答下列问题:
(1)步骤①所得废渣的成分是 (写化学式),操作I的名称 。
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):
R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是 。③中X试剂为 。
(3)⑤的离子方程式为 。
(4)25℃时,取样进行试验分析,得到钒沉淀率和溶液pH之间关系如下表:
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
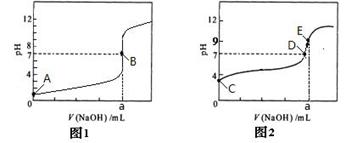
常温下,将a mL 三种一元酸分别和NaOH溶液等体积混合,实验数据如下:
| 组别 | c(一元酸) | c(NaOH) /mol/L | 混合溶液的pH |
| 甲 | c(HX)=0.1 mol/L | 0.1 | pH = x |
| 乙 | c(HY)=0.1mol/L | 0.1 | pH = 7 |
| 丙 | c(HZ)=0.1 mol/L | 0.1 | pH = 9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com