
����Ŀ����2 L���ܱ������з�����ӦxA(g)��yB(g)![]() zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ���ǣ� ����
zC(g)��ͼ�ױ�ʾ200 ��ʱ������A��B��C���ʵ�����ʱ��ı仯��ͼ�ұ�ʾ��ͬ�¶���ƽ��ʱC�������������ʼn(A)��n(B)�ı仯��ϵ�������н�����ȷ���ǣ� ����

A. 200 ��ʱ����Ӧ�ӿ�ʼ��ƽ���ƽ������v(B)��0.04 mol��L��1��min��1
B. 200��ʱ���÷�Ӧ��ƽ�ⳣ��Ϊ25 L2/mol2
C. �����������200�����µ�100����ԭƽ��һ�����ƻ��������淴Ӧ���ʾ�����
D. ��ͼ�ҿ�֪����ӦxA(g)��yB(g)![]() zC(g)����H<0����a��2
zC(g)����H<0����a��2
���𰸡�B
����������ͼ��֪����Ӧ��A��B��C�����ʵ����ı仯��Ϊ0.4��0.2��0.2=2��1��1�����ݷ�Ӧ�м�����֮�ȵ������ʵ����ʵ����ı仯��֮�ȿ�֪���÷�Ӧ����ʽΪ��2A��g��+B��g��![]() C��g����A������v=
C��g����A������v=![]() ��֪v��B��=
��֪v��B��=![]() molL-1min-1=0.02molL-1min-1����A����B����ͼ��֪ƽ��ʱA��B��C�����ʵ����ֱ�Ϊ0.4mol��0.2mol��0.2mol���������ǵ�Ũ�ȷֱ�Ϊ��0.2mol/L��0.1mol/L��0.1mol/L����ϻ�ѧ����ʽ2A��g��+B��g��
molL-1min-1=0.02molL-1min-1����A����B����ͼ��֪ƽ��ʱA��B��C�����ʵ����ֱ�Ϊ0.4mol��0.2mol��0.2mol���������ǵ�Ũ�ȷֱ�Ϊ��0.2mol/L��0.1mol/L��0.1mol/L����ϻ�ѧ����ʽ2A��g��+B��g��![]() C��g������֪�÷�Ӧ��ƽ�ⳣ��Ϊ
C��g������֪�÷�Ӧ��ƽ�ⳣ��Ϊ![]() L2/mol2=25L2/mol2����B��ȷ��C������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ�����������¶�ƽ�������ƶ���ͬʱ��Ӧ��������C����D������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ����H��0����Ͷ��ķ�Ӧ������ʵ���֮�ȵ��ڻ�ѧ��Ӧ�м�����֮��ʱ��ƽ��ʱC��������������ֵ�����ݻ�ѧ����ʽ2A��g��+B��g��C��g������֪a=2����D����ѡB��
L2/mol2=25L2/mol2����B��ȷ��C������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ�����������¶�ƽ�������ƶ���ͬʱ��Ӧ��������C����D������ͼ�ҿ�֪�������¶ȣ�C�������������ƽ�������ƶ�����������ӦΪ���ȷ�Ӧ����H��0����Ͷ��ķ�Ӧ������ʵ���֮�ȵ��ڻ�ѧ��Ӧ�м�����֮��ʱ��ƽ��ʱC��������������ֵ�����ݻ�ѧ����ʽ2A��g��+B��g��C��g������֪a=2����D����ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������ͼװ�ý����к��ȵIJⶨ���ش��������⣺ 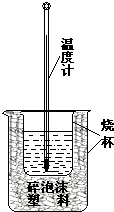
��1����ͼװ���У�Ϊ������ܸ���ֵط�Ӧ��Ӧ������һ��������������ƣ������ձ���û�и���Ӳֽ�壬��õ��к�����ֵ�������ƫ����ƫС������Ӱ�족����
��2���ڲ�����ȷ��ǰ��������к��Ȳⶨ��ȷ�ԵĹؼ����� ����ţ�
A.����ʵ��ʱ������
B.װ�õı��¸���Ч��
C.ʵ�����������Һ�����
��3�������0.5 mol/L��������������ƹ������ʵ�飬��ʵ����������ġ��к��ȡ�����ֵ�����ƫ����ƫС���������䡱����ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ͼһ��ʾ���ǿ��淴ӦA(g)��B(g)![]() C(s)��D(g)����H>0�Ļ�ѧ��Ӧ����(v)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2NO2(g)
C(s)��D(g)����H>0�Ļ�ѧ��Ӧ����(v)��ʱ��(t)�Ĺ�ϵ��ͼ����ʾ���ǿ��淴Ӧ2NO2(g)![]() N2O4(g)����H<0��Ũ��(c)��ʱ��t�ı仯���������˵������ȷ����
N2O4(g)����H<0��Ũ��(c)��ʱ��t�ı仯���������˵������ȷ����

A. ��ͼһt2ʱ�ı������������ѹǿ����Ӧ�Ħ�H����
B. ͼһt2ʱ�ı�������������������¶Ȼ�������ѹǿ
C. ͼ��t1ʱ�ı�������������������¶Ȼ�������ѹǿ
D. ��ͼ��t1ʱ�ı������������ѹǿ�����������ƽ����Է�����������С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�CO2�����öԴٽ���̼���Ĺ���������Ҫ������
��1����CO2�뽹̿��������CO��CO��������������
��֪��
Fe2O3��s��+3CO��s��ʯī���T2Fe��s��+3CO2��g����H1=+489.0kJmol��1
C��s��ʯī��+CO2��g���T2CO��g����H2=+172.5kJmol��1
��CO��ԭFe2O3��s�����Ȼ�ѧ����ʽΪ_____��
��2��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��CO2��g��+3H2��g��![]() CH3OH��g��+H2O��g����H
CH3OH��g��+H2O��g����H
��ȡһ�����CO2��H2�Ļ�����壨���ʵ���֮��Ϊ1��3������������ܱ������У�����������Ӧ��Ӧ�����в�ü״�����������գ�CH3OH���뷴Ӧ�¶�T�Ĺ�ϵ��ͼ1��ʾ����÷�Ӧ�ġ�H____0�����������������=������ͬ����
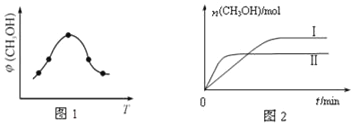
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ2��ʾ������I������Ӧ��ƽ�ⳣ����ϵΪK��_____K����
��3����CO2Ϊԭ�ϻ����Ժϳɶ���������
�ٹ�ҵ������[CO��NH2��2]��CO2��NH3��һ�������ºϳɣ���ʼ��̼��![]() =3���з�Ӧ����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ_____��
=3���з�Ӧ����ƽ��ʱCO2��ת����Ϊ60%����NH3��ƽ��ת����Ϊ_____��
�ڽ�����CO2ͨ�뱥�Ͱ�ˮ�пɵõ���NH4HCO3����֪������һˮ�ϰ�Kb=1.8��10��5��̼��һ�����볣��Ka=4.3��10��7����NH4HCO3��Һ��_____������ԡ��������ԡ����ԡ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.1000mol/L������ζ�20.00mLδ֪Ũ�ȵ�Na2CO3��Һ����Һ��pH����������������ϵ��ͼ��ʾ�������й�������ȷ���ǣ� ��

A. c�㴦����Һ��c(Na+)��c(Cl��)��c(HCO![]() )��2c(CO
)��2c(CO![]() )
)
B. a����Һ�ʼ��Ե�ԭ�������ӷ���ʽ��ʾΪ�� CO![]() ��2H2O
��2H2O![]() H2CO3��2OH��
H2CO3��2OH��
C. b����Һ��c(Na+)> c(HCO![]() )> c(Cl��)
)> c(Cl��)
D. d�㴦��Һ��ˮ�ĵ���̶ȴ���b�㴦
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʼ��ת����ϵ��ȷ���ǣ� ��
A.FeCl2��aq�� ![]() FeCl3��aq��
FeCl3��aq�� ![]() FeCl2��aq��
FeCl2��aq��
B.H2SO3 ![]() Si02
Si02 ![]() SiCl4
SiCl4
C.NaCl��aq�� ![]() NaHC03��s��
NaHC03��s�� ![]() Na2CO3��s��
Na2CO3��s��
D.CuS04 ![]() Cu��OH��2
Cu��OH��2 ![]() Cu
Cu
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и������ʰ��ᡢ��η���˳��������ȷ����
A. ���ᡢ���ʯ�� B. ̼�ᡢ�Ҵ���������
C. �����ᡢ�ռ���� D. ���ᡢ��ʯ�ҡ����Լ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪CuSO4��Һ�ֱ���Na2CO3��Һ��Na2S��Һ�ķ�Ӧ���������
(1)CuSO4+Na2CO3
��Ҫ��Cu2++CO32��![]() +H2O��Cu(OH)2��+CO2�� ��Ҫ��Cu2++ CO32����CuCO3��
+H2O��Cu(OH)2��+CO2�� ��Ҫ��Cu2++ CO32����CuCO3��
(2)CuSO4+Na2S
��Ҫ��Cu2++S2����CuS�� ��Ҫ��Cu2++S2��+2H2O��Cu(OH)2��+H2S��
���м������ʵ��ܽ�ȴ�С�ıȽ�������ȷ����( )
A. Cu(OH)2>CuCO3>CuS B. CuS>Cu(OH)2>CuCO3
C. CuS<Cu(OH)2<CuCO3 D. Cu(OH)2<CuCO3<CuS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڷ�Ӧ8NH3+3Cl2��6NH4Cl+N2�У���ԭ���ͻ�ԭ��������ʵ���֮����
A.1:3B.3:1C.1:1D.3:8
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com