
【题目】温度为T1时,在三个容积均为1 L的恒容密闭容器中仅发生反应: 2NO2(g)![]() 2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
2NO(g)+O2(g) (正反应吸热)。实验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗= 2v(O2)消耗=k逆c2(NO)·c(O2),k正、k逆为速率常数,受温度影响。下列说法正确的是
容器编号 | 物质的起始浓度(mol/L) | 物质的平衡浓度(mol/L) | ||
c (NO2) | c (NO) | c (O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.3 | 0.5 | 0.2 | |
Ⅲ | 0 | 0.5 | 0.35 | |
A. 达平衡时,容器Ⅰ与容器Ⅱ中的总压强之比为4∶5
B. 达平衡时,容器Ⅱ中c(O2)/ c(NO2)比容器Ⅰ中的大
C. 达平衡时,容器Ⅲ中NO的体积分数小于50%
D. 当温度改变为T2时,若k正=k逆,则T2>T1
【答案】CD
【解析】由容器Ⅰ中反应2NO2![]() 2NO+O2
2NO+O2
起始量(mol/L) 0.6 0 0
变化量(mol/L) 0.4 0.4 0.2
平衡量(mol/L) 0.2 0.4 0.2
可以求出平衡常数K=![]() =0.8,平衡时气体的总物质的量为0.8mol,其中NO占0.4mol,所以NO的体积分数为50%,c(O2)/ c(NO2)=1。在平衡状态下,v正= v (NO2)消耗= v逆= v(NO)消耗,所以k正c2(NO2) = k逆c2(NO)·c(O2),进一步求出
=0.8,平衡时气体的总物质的量为0.8mol,其中NO占0.4mol,所以NO的体积分数为50%,c(O2)/ c(NO2)=1。在平衡状态下,v正= v (NO2)消耗= v逆= v(NO)消耗,所以k正c2(NO2) = k逆c2(NO)·c(O2),进一步求出![]() =K=0.8。
=K=0.8。
A、显然容器Ⅱ的起始投料与容器Ⅰ的平衡量相比,增大了反应物浓度,平衡将向正反应方向移动,所以容器Ⅱ在平衡时气体的总物质的量一定小于1mol,故两容器的压强之比一定大于4:5,A错误;若容器II在某时刻,c(O2)/ c(NO2)=1,
由反应2NO2![]() 2NO + O2
2NO + O2
起始量(mol/L) 0.3 0.5 0.2
变化量(mol/L) 2x 2x x
平衡量(mol/L) 0.3-2x 0.5+2x 0.2+x
因为,![]() ,解之得x=
,解之得x=![]() ,求出此时浓度商Qc=
,求出此时浓度商Qc= >K,所以容器II达平衡时,c(O2)/ c(NO2)一定小于1,B错误;
>K,所以容器II达平衡时,c(O2)/ c(NO2)一定小于1,B错误;
C. 若容器III在某时刻,NO的体积分数为50%,
由反应2NO2![]() 2NO + O2
2NO + O2
起始量(mol/L) 0 0.5 0.35
变化量(mol/L) 2x 2x x
平衡量(mol/L) 2x 0.5-2x 0.35-x
由0.5-2x=2x+0.35-x,解之得x=0.05,求出此时浓度商Qc=![]() =4.8>K,说明此时反应未达平衡,反应继续向逆反应方向进行,NO进一步减少,所以C正确;
=4.8>K,说明此时反应未达平衡,反应继续向逆反应方向进行,NO进一步减少,所以C正确;
D.温度为T2时,![]() =K2=1>0.8,因为正反应是吸热反应,升高温度后化学平衡常数变大,所以T2>T1,
=K2=1>0.8,因为正反应是吸热反应,升高温度后化学平衡常数变大,所以T2>T1,


科目:高中化学 来源: 题型:
【题目】“一碳化学”是以分子中只含一个碳原子的化合物(如CO、CH4等)为原料来合成一系列化工原料和燃料的化学。发展“一碳化学”,开发利用我国相对丰富的煤炭资源具有重要的战略意义和经济价值。下面是以焦炭为原料,经“一碳化学”途径制取乙二醇的过程:
(1)在容积为2L的密闭容器中,由CO和H2合成乙醇的反应为
2CO(g)+ 4H2(g)![]() CH3CH2OH(g)+ H2O(g),在其他条件不变的情况下,CO的转化率随温度的变化如图所示(注:T1、T2均大于280℃):
CH3CH2OH(g)+ H2O(g),在其他条件不变的情况下,CO的转化率随温度的变化如图所示(注:T1、T2均大于280℃):
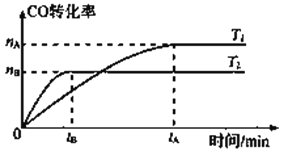
①根据上图可推知该反应ΔH_________0(填“>”、“<”或“=”)。
②该反应的平衡常数表达式为____________,降低温度平衡常数将_____(填“变大”、“变小”或“不变”)。
③下列说法中能判断该反应达到化学平衡状态的是_________(选填编号)。
a.容器中的压强不变 b.混合气体的密度不再变化
c.v正(CO)=2v逆(H2O) d.混合气体的平均相对分子质量不再变化
(2)草酸二甲酯水解产物草酸(H2C2O4)为二元中强酸
①用离子方程式解释KHC2O4溶液显酸性的原因:_______________。
②向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是________(填序号)。
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)
b.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-)
c.c(Na+)=c(H2C2O4)+c(C2O42-)
d.c(K+)>c(Na+)
(3)CH3OH(l)气化时吸收的热量为27kJ/mol,CH3OH(g)的燃烧热为677kJ/mol,请写出CH3OH(l)完全燃烧的热化学方程式______________________________。以甲醇为原料,使用酸性电解质构成燃料电池,该燃料电池的负极反应式为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得101kPa时,1mol H2(g)完全燃烧生成液态水,放出285.8kJ的热量;1mol CH4(g)完全燃烧生成液态水和CO2气体,放出890.3kJ的热量.下列热化学方程式书写正确的是( )
A.2H2(g)+O2(g)═2H2O(l)△H=﹣285.8 kJ/mol
B.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890.3 kJ/mol
C.CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890.3 kJ/mol
D.CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=+890.3 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A与CO、H2O以物质的量1︰1︰1的比例形成B,B中的两个官能团分别具有乙烯和乙酸中官能团的性质,E是有芳香气味、不易溶于水的油状液体,有关物质的转化关系如下:
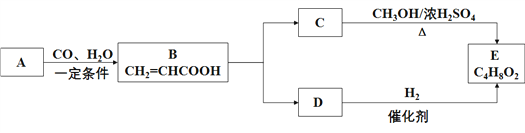
请回答:
(1)A的结构简式__________。
(2)D→E的反应类型__________。
(3)CE的化学方程式________________________________________。
(4)下列说法不正确的是__________。
A.可用金属钠鉴别B和C
B.A在一定条件下可与氯化氢发生加成反应
C.乙酸和乙醇在浓硫酸作用下加热也可生成E
D.与A的最简式相同,相对分子质量为78的烃一定不能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的工作原理为:Pb+PbO2+2H2SO4═2PbSO4+2H2O,研读图,下列判断不正确的是
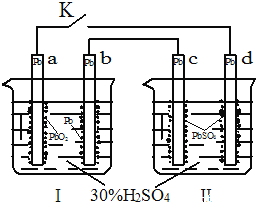
A. K闭合时,d电极反应式:PbSO4+2H2O-2e-═PbO2+4H++SO42-
B. 当电路中转移0.2mol电子时,I中消耗的H2SO4为0.2mol
C. K闭合时,II中SO42-向c电极迁移
D. K闭合一段时间后,II可单独作为原电池,d电极为正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1902年德国化学家哈伯研究出合成氨的方法.
(1)某温度时,N2与H2反应(可逆反应)过程中的能量变化如图1所示. 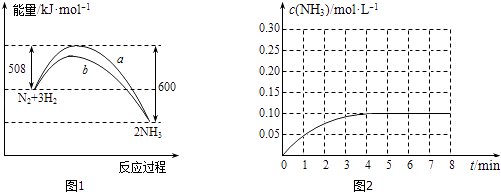
①写出合成氨的热化学方程式 .
②下列叙述正确的是 .
A.b曲线是加入催化剂时的能量变化曲线
B.在密闭容器中加入28gN2、6gH2 , 充分反应放出的热量小于92kJ
C.由图可知,断开1molN≡N键与3molH﹣H键吸收的能量和小于形成6molN﹣氮氢键所放出的能量
D.反应物的总能量低于生成物的能量
(2)在一容积为4L的密闭容器中,加入0.4molN2和1.2molH2 , 在一定条件下发生反应,反应中NH3的物质的量浓度变化情况如图2所示.据图计算从反应开始到平衡时,平均反应速率(H2)为mol/(Lmin),平衡时,c(N2)为 .
(3)哈伯因证实N2、H2在固体催化剂(Fe)表面吸附和解吸以合成氨的过程而获诺贝尔奖.若用 ![]() 分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是(填字母序号).
分别表示N2、H2、NH3和固体催化剂,则在固体催化剂表面合成氨的过程可用如图表示.吸附后,能量状态最高的是(填字母序号). 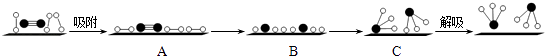
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代以石油化工为基础的三大合成材料是
①合成氨 ②塑料 ③医药 ④合成橡胶 ⑤合成尿素 ⑥合成纤维 ⑦合成洗涤剂
A.①③⑤B.②④⑥C.②④⑦D.④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com