
【题目】环戊二烯可用于制备二茂铁(Fe(C5H5)2,结构简式为 ),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法错误的是( )
),后者广泛应用于航天、化工等领域中。二茂铁的电化学制备原理如图所示,其中电解液为溶解有溴化钠(电解质)和环戊二烯的DMF溶液(DMF为惰性有机溶剂)。下列说法错误的是( )


A.制备二茂铁总反应为:Fe+2![]() =
=![]() +H2↑
+H2↑
B.电解制备需要在无水条件下进行
C.Ni电极与电源负极连接
D.阳极电极反应为:2Br--2e-=Br2
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移电子总数为0.1mol
B.明矾溶于水形成的Al(OH)3胶体能吸附水中悬浮物,所以明矾可用于水的净化
C.向Na2CO3溶液中滴加盐酸溶液,一定有CO2气体生成
D.Na2O2常用于潜水艇或呼吸面具的供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作及现象推出的结论正确的是
| 实验操作 | 实验现象 | 实验结论 |
A. | 向某溶液中滴加少量氯水,再滴加淀粉溶液 | 溶液变为蓝色 | 则原溶液中一定含 |
B. | 向某盐溶液中滴加浓盐酸,将产生的气体通入品红溶液中 | 品红溶液褪色 | 该盐一定是亚硫酸盐或亚硫酸氢盐 |
C. | 将浓盐酸与石灰石混合,产生的气体通入 | 出现白色沉淀 | C的非金属性比Si强 |
D. | 加热涂有石蜡油的碎瓷片,将生成的气体通入酸性 |
| 石蜡油分解产生不饱和烃 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂是一种常见的心血管疾病,治疗高血脂的新药I的合成路线如下:

已知:a、
b、
![]() RCHO
RCHO
回答下列问题:
(1)反应①所需试剂、条件分别是____________;A的化学名称为____________。
(2)②的反应类型是______________;A→B 的化学方程式为_________________。
(3)E的结构简式为______________;I 中所含官能团的名称是____________。
(4)化合物W 的相对分子质量比化合物C 大14,且满足下列条件①遇FeCl3 溶液显紫色;②能发生银镜反应,W 的可能结构有____种。其中核磁共振氢谱显示有5 种不同化学环境的氢,峰面积比为2:2:2:1:1,写出符合要求的W 的结构简式________。
(5)设计用甲苯和乙醛为原料制备 ![]() 的合成路线,其他无机试剂任选(合成路线常用的表示方式为A
的合成路线,其他无机试剂任选(合成路线常用的表示方式为A![]() B
B![]() 目标产物。____________
目标产物。____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终点。在一定温度下,用0.1mol/LKOH溶液分别滴定体积均为20mL、浓度均为0.1mol/L的盐酸和醋酸溶液,滴定曲线如图所示。下列有关判断正确的是

A. B点的溶液中有:c(K+)>c(OH-)>c(CH3COO-)>c(H+)
B. A点的溶液中有:c(CH3COO-)+c(OH-)-c(H+)=0.1mol/L
C. C点水电离的c(OH-)大于A点水电离的c(OH-)
D. A、B、C三点溶液均有Kw=c(H+)·c(OH-)=1.0×10-14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为N2(g)和 O2(g)反应生成 NO(g)过程中的能量变化,下列正确的是( )
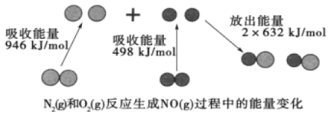
A.1molN2(g) 和 NA 个 O2(g) 反 应 放 出 的 能 量 为 180 kJ
B.1molN2(g)和 1molO2(g)具有总键能小于 2molNO(g)具有的总键能
C.该反应的热化学方程式为:N2(g)+ O2(g)= 2NO(g)△H=+180 kJmol﹣1
D.吸热反应一定需要加热才能发生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体界面上强酸的吸附和离解是多相化学在环境、催化、材料科学等领域研究的重要课题。下图为少量HCl气体分子在253 K冰表面吸附和溶解过程的示意图。下列叙述错误的是

A. 冰表面第一层中,HCl以分子形式存在
B. 冰表面第二层中,H+浓度为5×103 mol·L1(设冰的密度为0.9 g·cm3)
C. 冰表面第三层中,冰的氢键网格结构保持不变
D. 冰表面各层之间,均存在可逆反应HCl![]() H++Cl
H++Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是自然界碳循环中的重要物质。下列过程会引起大气中CO2含量上升的是
A. 光合作用 B. 自然降雨
C. 化石燃料的燃烧 D. 碳酸盐的沉积
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:常温下,Ksp(CuS)=1.0×10-36,K sp(HgS)=1.6×10-52;pM=-lgc(M2+)。常温下,向10.0mL0.20mol·L-1Cu(NO3)2溶液中逐滴滴加0.10mo l·L-1Na2S溶液,溶液中pM与加入Na2S溶液的体积(V)的关系如图所示。下列说法错误的是

A. V0=20.0mL,m=18
B. 若c[Cu(NO3)2]=0.01mol·L-1,则反应终点可能为e点
C. a、b、d三点中,由水电离的c(H+)和c(OH-)的积最大的为b点
D. 相同条件下,若用等浓度等体积的Hg(NO3)2溶液代替上述Cu(NO3)2溶液,则反应终点b向c方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com