
【题目】某有机物结构简式如图,下列关于该有机物的说法正确的是
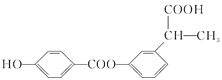
A. 1 mol 该有机物含有 6 mol 碳碳双键
B. 1 mol 该有机物完全燃烧可生成9 mol H2O
C. 1 mol 该有机物可电离生成2 mol H+
D. 1 mol 该有机物最多可与6 mol H2 发生加成反应
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1,图2所示的实验。下列叙述中不正确的是( )
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②, 则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子中,在水溶液中能大量共存,且无色透明的是
A.Na+、Ba2+、NO3-、CO32-B.Cu2+、HCO3-、C1-、K+
C.Na+、K+、HCO3-、SO42-D.OH-、Cl-、Na+、Mg2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生活、生产中有广泛应用。
(1)常用胆矾溶液对游泳池中的水消毒,它的水溶液呈酸性,用离子方程式表示其原因:________________________________________________________________________________。
(2)在Cu(OH)2悬浊液中滴加氨水,蓝色沉定变成蓝色溶液。已知:Ksp[Cu(OH)2]=2.2×10-20,Cu2+(aq)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)K1=2.0×1013。则
[Cu(NH3)4]2+(aq)K1=2.0×1013。则
Cu(OH)2(s)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
[Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
(3)Cu(OH)2溶于浓烧碱溶液生成Na2CuO2,在Na2CuO2溶液中滴加CuCl2溶液,可能观察到的现象是______________________________________________________________________________。
(4)纳米级氧化亚铜(Cu2O)常作催化剂。工业上可用电解法制备,装置如图所示。
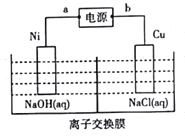
①a极名称是_________________;阳极的反应式为___________________。
②若电解过程中有1mol离子通过交换膜,则制备Cu2O的质量为_____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一未知的无色溶液,只可能含有以下离子中的若干种:NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、SO42- , 现取两份100mL溶液进行如下实验: ①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。以下推测不正确的是( )
A.原溶液一定不存在Cu2+
B.不能确定原溶液是否含有K+
C.实验所加的NaOH的浓度为2mol·L-1
D.原溶液确定含Mg2+、Al3+、NH4+ , 且n(Mg2+) ∶n(Al3+)∶n( NH4+)=1∶1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g) ![]() C(g)+D(g),5 min后达到平衡.已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
C(g)+D(g),5 min后达到平衡.已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
A.a=3
B.a=2
C.B的转化率为40%
D.B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用特殊方法把固体物质加工到纳米级(1nm—100nm)的超细粉末粒子,然后制得纳米材料。下列分散质粒子直径具有与此相同数量级的是( )
A.淀粉溶液B.泥水C.酒精D.硫酸铜溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据左表中数据,在图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线: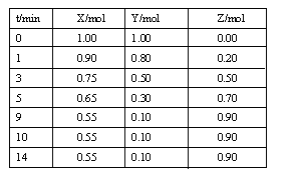
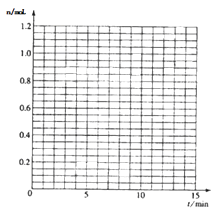
(2)体系中发生反应的化学方程式是;
(3)列式计算该反应在0-3min时间内产物Z的平均反应速率;
(4)该反应达到平衡时反应物X的转化率α等于;
(5)如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如下图所示)。则曲线①、②、③所对应的实验条件改变分别是:① ②③。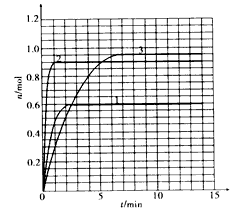
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有浓度均为0.1 mol/L的下列溶液:①硫酸②醋酸③氢氧化钠④氯化铵,请回答下列问题:
(1)①②③④四种溶液中促进水的电离的物质是(填序号)。
(2)①②③④四种溶液中pH由大到小的顺序是(填序号)。
(3)将②和③等体积混合后,混合液中各离子浓度由大到小的顺序是。
(4)25℃时,将pH=13的NaOH溶液aL与pH=2的H2SO4溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=12,则a:b=。
(5)将a mol/L的氨水溶液与①等体积混合后,溶液呈中性,则氨水的电离平衡常数Kb=。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com