
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1,图2所示的实验。下列叙述中不正确的是( )
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②, 则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
【答案】B
【解析】A、反应的剧烈程度与实验现象有关,反应越剧烈,产生气体的速率越快,产生气泡越快,A不符合题意;
B、催化剂能改变化学反应的速率,这里是加快速率,若图1所示实验中反应速率为①>②,则一定说明氯化铁比硫酸铜催化效果好,因二者所含的阴离子不同,要证明Fe3+比Cu2+对H2O2分解催化效果好,还要使选择的试剂中阴离子种类相同,B符合题意;
C、反应速率可用单位时间内产生的气体体积表示,该装置可通过注射器活塞的位置变化看生成气体的体积,C不符合题意;
D、检查装置的气密性一般是利用气压的原理,在图2装置中,关闭A处活塞,将注射器的活塞拉出一定距离,过一段时间后再松开活塞,如活塞回到原位,说明气密性良好,否则漏气,D不符合题意;
故答案为:BA.催化剂可改变反应速率,而反应速率的快慢可通过产生气泡的快慢判断;
B.图①中所用溶液溶质的阴离子不同,有可能是阴离子起到催化剂作用;
C.反应速率的快慢可用单位时间内产生气体的体积表示,注射器可用于确定产生气体的体积;
D.若装置不漏气,则注射器活塞会恢复至原来的状态;


科目:高中化学 来源: 题型:
【题目】在实验室中,下列除杂![]() 括号内物质为杂质
括号内物质为杂质![]() 的方法正确的是
的方法正确的是![]()
![]()
A. 溴苯(溴):加入KI溶液,振荡,分液
B. 乙烷(乙烯):通过盛有![]() 溶液的洗气瓶
溶液的洗气瓶
C. 硝基苯(浓HNO3):将其倒入足量NaOH溶液中,振荡、静置,分液
D. 乙烯(SO2):通过盛有溴水的洗气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(B)=0.3mol/(L· s) B. v(A)=0.5mol/(L· min)
C. v(C)=0.8mol/(L· s) D. v(D)=1mol/(L· min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2 , 在相同温度下发生反应:2SO2+ O2 ![]() 2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A.等于p%
B.大于p%
C.小于p%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关铁盐溶液的叙述,正确的是
A. Fe2(SO4)3溶液中:K+、Fe2+、C6H5OH、Br-可以大量共存
B. Fe2(SO4)3溶液和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-==Fe(OH)3↓+BaSO4↓
C. FeBr3溶液中滴加KI-淀粉溶液变为蓝色
D. FeBr3溶液与硝酸酸化的AgNO3溶液反应有沉淀生成并放出气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)——空气燃料电池的工作原理如图所示。电池工作时,下列说法不正确的是
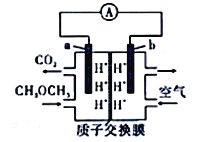
A. b极反应式:O2+H2O+4e-==4OH-
B. a极反应式:CH3OCH3+3H2O-12e-==2CO2↑+12H+
C. b极区溶液的pH变大
D. 每消耗1mol CH3OCH3,有12mol H+向右侧移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.氢气的摩尔质量是2g/mol
B.标准状态下22.4L水的物质的量是1mol
C.常温常压下氢气的摩尔体积是22.4L/mol
D.常温常压下16gO2的物质的量是1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,下列关于该有机物的说法正确的是
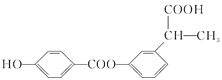
A. 1 mol 该有机物含有 6 mol 碳碳双键
B. 1 mol 该有机物完全燃烧可生成9 mol H2O
C. 1 mol 该有机物可电离生成2 mol H+
D. 1 mol 该有机物最多可与6 mol H2 发生加成反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com