
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(B)=0.3mol/(L· s) B. v(A)=0.5mol/(L· min)
C. v(C)=0.8mol/(L· s) D. v(D)=1mol/(L· min)
【答案】A
【解析】
反应速率之比等于化学计量数之比,则反应速率与化学计量数的比值越大,反应速率越快,以此来解答。
反应速率与化学计量数的比值越大,反应速率越快,则
A、v(B)/1=0.3mol/(L·s)÷1=0.3mol/(L·s);
B、v(A)/2=0.5mol/(L·min)÷2=0.25mol/(L·min)=0.0042 mol/(L·s);
C、v(C)/3=0.8mol/(L·s)÷3=0.26 mol/(L·s);
D、v(D)/4=1 mol/(L·min)÷4=0.25 mol/(L·min)=0.042 mol/(L·s)。
显然选项A中比值最大,反应速率最快。
答案选A。


 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)为一元弱酸,广泛用于玻璃、医药、冶金、皮革等工业。回答下列问题:
(1) H3BO3中B元素的化合价为______,其在元素周期表的位置是_________________。
(2)已知:A(OH)3+H2O![]() [Al(OH)4]-+H+,H3BO3的电离方程式为_______。酸性:H3BO3 _____(填*>”或“<”)Al(OH)3。
[Al(OH)4]-+H+,H3BO3的电离方程式为_______。酸性:H3BO3 _____(填*>”或“<”)Al(OH)3。
(3) H3BO3受热分解得到的B2O3和镁粉混合点燃可得单质B,生成单质B的化学方程式为________。
(4) H3BO3可用于生产储氢材料NaBH4。涉及的主要反应为:
I.H3BO3+3CH3OH→B(OCH3)3+3H2O
II.B(OCH3)3+4NaH→NaBH4+3CH3ONa
①“反应I”的类型为__________(填标号)。
A.取代反应 B.加成反应 C.加聚反应 D.氧化反应
②NaH的电子式为_______________。
③在碱性条件下,NaBH4与CuSO4溶液反应可得Cu和Na[B(OH)4],其中H元素由-1价升高为+1价,该反应的离子方程式为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水中的电离方程式是H2A = H+ + HA﹣ , HA﹣ ![]() H+ + A2﹣ . 回答下列问题:
H+ + A2﹣ . 回答下列问题:
(1)Na2A溶液显(填“酸性”、“中性”或“碱性”),理由是(用离子方程式或必要的文字说明).
(2)常温下,已知0.1molL﹣1NaHA溶液pH=2,则0.1molL﹣1H2A溶液中氢离子的物质的量浓度可能0.11molL﹣1(填“大于”、“等于”或“小于”),理由是 .
(3)0.1molL﹣1NaHA溶液中各种离子浓度由大到小的顺序是 .
(4)Na2A溶液中,下列表述正确的是_________.
A.c(Na+)+ c(H+)= c(HA﹣)+ 2c(A2﹣)+ c(OH﹣)
B.c(OH﹣)= c(HA﹣)+ c(H+)
C.c(OH﹣)= c(HA﹣)+ c(H+)+ 2c(H2A)
D.c (Na+)= 2[c(HA﹣)+ c(A2﹣) + c(H2A)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( ) 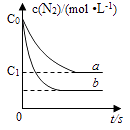
A.温度T下,该反应的平衡常数K= ![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如下,其中正确的是 ( )
A.①②③
B.②④
C.①③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产、材料和环境关系非常密切,下列说法不正确的是
A. 将草木灰与NH4H2PO4混合施用可更好地为植物全面提供N、P、K 三种营养元素
B. 酸雨以及光化学烟雾的形成通常都与氮的含氧化合物有关
C. 金刚砂和氧化铝透明陶瓷都属于无机非金属材料
D. 用K2FeO4代替Cl2处理饮用水,既能杀菌又能净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1,图2所示的实验。下列叙述中不正确的是( )
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②, 则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)===2LiH(s) ΔH=-182 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1;
③4Li(s)+O2(g)===2Li2O(s) ΔH=-1196 kJ·mol-1。
试写出LiH在O2中燃烧的热化学方程式:__________________________________________。
(II)利用H2和CO2生产甲醇。某温度下,在容积为2L的密闭容器中充入1molCO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
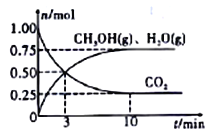
(1)从反应开始到3min时,氢气的平均反应速率v(H2)=____________。
(2)下列措施中一定能使CO2的转化率增大的是_______________(填序号)。
A.在原容器中再充入1mol CO2 B.在原容器中再充入1mol H2
C.在原容器中再充入1mol He D.使用更有效的催化剂
E. 缩小容器的容积 F. 将水蒸气从体系中分离出
(III)图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
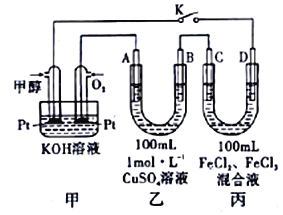
(1)甲中负极的电极反应式为_______________________________。
(2)乙中A极析出的气体在标准状况下的体积为_______________________。
(IV)已知常温下CN-的水解常数Kb=1.61×10-5。
(1)常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_________(填“酸”“碱”或“中”)性,c(CN-)_______(填“>”“<”或“=”)c(HCN)。
(2)常温下,若将c molL-1盐酸与0.61 molL-1KCN溶液等体积混合后恰好得到中性溶液,则c=________(小数点后保留4位数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜及其化合物在生活、生产中有广泛应用。
(1)常用胆矾溶液对游泳池中的水消毒,它的水溶液呈酸性,用离子方程式表示其原因:________________________________________________________________________________。
(2)在Cu(OH)2悬浊液中滴加氨水,蓝色沉定变成蓝色溶液。已知:Ksp[Cu(OH)2]=2.2×10-20,Cu2+(aq)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)K1=2.0×1013。则
[Cu(NH3)4]2+(aq)K1=2.0×1013。则
Cu(OH)2(s)+4NH3(aq)![]() [Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
[Cu(NH3)4]2+(aq)+2OH-(aq)K2=_____________。
(3)Cu(OH)2溶于浓烧碱溶液生成Na2CuO2,在Na2CuO2溶液中滴加CuCl2溶液,可能观察到的现象是______________________________________________________________________________。
(4)纳米级氧化亚铜(Cu2O)常作催化剂。工业上可用电解法制备,装置如图所示。
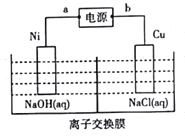
①a极名称是_________________;阳极的反应式为___________________。
②若电解过程中有1mol离子通过交换膜,则制备Cu2O的质量为_____________g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com