
【题目】分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如下,其中正确的是 ( )
A.①②③
B.②④
C.①③
D.①②③④
【答案】A
【解析】①随着反应的进行,氢离子浓度逐渐减小但是醋酸会逐渐电离出氢离子,所以醋酸中氢离子消耗的速率慢,正确;
②等pH时,醋酸浓度较大,加入足量锌,不仅产生的氢气的体积更大,而且反应更快,正确;
③等浓度的盐酸和醋酸,盐酸的pH小,和金属锌反应的速率比醋酸的快正确;
④等浓度的盐酸和醋酸,因为盐酸是强酸,醋酸是弱酸,盐酸中H+浓度大,和金属锌反应的速率是盐酸比醋酸的快,错误;
所以答案是:A
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


科目:高中化学 来源: 题型:
【题目】下面两种气体的原子数一定相等的是( )
A.质量相等,密度不同的氮气和一氧化碳
B.体积相等,密度相等的氮气和氢气
C.在温度相同、体积相等的条件下氧气和氮气
D.在压强相同、体积相等的条件下氧气和氮气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法正确的是![]()
![]()
A. 1mol苯分子中含有C=C双键数目为3NA
B. 标准状况下,11.2LCCl4中含有的共价键数目为2NA
C. 1mol乙烯和乙醇的混合物完全燃烧时消耗O2的分子数为3NA
D. 常温常压下,17g羟基含有的电子总数为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有三组溶液:①含有水份的植物油中除去水份②回收碘的CCl4溶液中的CCl4③用乙醚浸泡青蒿提取其中的有效成份青蒿素 ④除去食盐溶液中的泥沙。分离以上各混合液的正确方法依次是( )
A.分液、萃取、蒸馏、蒸发B.萃取、蒸馏、分液、过滤
C.分液、蒸馏、萃取、过滤D.蒸馏、萃取、分液、蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)反应中,表示该反应速率最快的是( )
3C(g)+4D(g)反应中,表示该反应速率最快的是( )
A. v(B)=0.3mol/(L· s) B. v(A)=0.5mol/(L· min)
C. v(C)=0.8mol/(L· s) D. v(D)=1mol/(L· min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2 , 在相同温度下发生反应:2SO2+ O2 ![]() 2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A.等于p%
B.大于p%
C.小于p%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)——空气燃料电池的工作原理如图所示。电池工作时,下列说法不正确的是
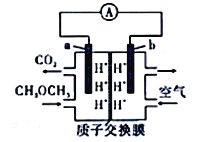
A. b极反应式:O2+H2O+4e-==4OH-
B. a极反应式:CH3OCH3+3H2O-12e-==2CO2↑+12H+
C. b极区溶液的pH变大
D. 每消耗1mol CH3OCH3,有12mol H+向右侧移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断 Na2SeO3的作用是( )
A.作还原剂B.作氧化剂C.既作氧化剂又作还原剂D.既不作氧化剂又不作还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com