
【题目】下列有关铁盐溶液的叙述,正确的是
A. Fe2(SO4)3溶液中:K+、Fe2+、C6H5OH、Br-可以大量共存
B. Fe2(SO4)3溶液和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-==Fe(OH)3↓+BaSO4↓
C. FeBr3溶液中滴加KI-淀粉溶液变为蓝色
D. FeBr3溶液与硝酸酸化的AgNO3溶液反应有沉淀生成并放出气体
科目:高中化学 来源: 题型:
【题目】有关甲烷和乙烷的说法中,错误的是
A.互为同系物
B.均不能使高锰酸钾酸性溶液褪色
C.在核磁共振氢谱图(1H核磁共振谱图)中,均只有1个吸收峰
D.二氯取代物均为两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,如图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化.下列叙述正确的是( ) 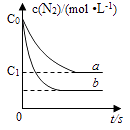
A.温度T下,该反应的平衡常数K= ![]()
B.温度T下,随着反应的进行,混合气体的密度减小
C.曲线b对应的条件改变可能是加入了催化剂
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产、材料和环境关系非常密切,下列说法不正确的是
A. 将草木灰与NH4H2PO4混合施用可更好地为植物全面提供N、P、K 三种营养元素
B. 酸雨以及光化学烟雾的形成通常都与氮的含氧化合物有关
C. 金刚砂和氧化铝透明陶瓷都属于无机非金属材料
D. 用K2FeO4代替Cl2处理饮用水,既能杀菌又能净水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1,图2所示的实验。下列叙述中不正确的是( )
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②, 则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(I)LiH可作飞船的燃料,已知下列反应:
①2Li(s)+H2(g)===2LiH(s) ΔH=-182 kJ·mol-1;
②2H2(g)+O2(g)===2H2O(l) ΔH=-572 kJ·mol-1;
③4Li(s)+O2(g)===2Li2O(s) ΔH=-1196 kJ·mol-1。
试写出LiH在O2中燃烧的热化学方程式:__________________________________________。
(II)利用H2和CO2生产甲醇。某温度下,在容积为2L的密闭容器中充入1molCO2和3.25mol H2,在一定条件下反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化关系如图所示。
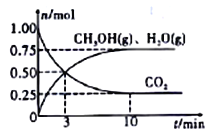
(1)从反应开始到3min时,氢气的平均反应速率v(H2)=____________。
(2)下列措施中一定能使CO2的转化率增大的是_______________(填序号)。
A.在原容器中再充入1mol CO2 B.在原容器中再充入1mol H2
C.在原容器中再充入1mol He D.使用更有效的催化剂
E. 缩小容器的容积 F. 将水蒸气从体系中分离出
(III)图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
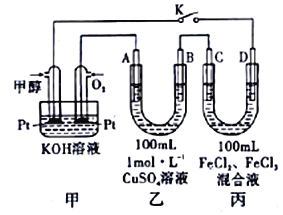
(1)甲中负极的电极反应式为_______________________________。
(2)乙中A极析出的气体在标准状况下的体积为_______________________。
(IV)已知常温下CN-的水解常数Kb=1.61×10-5。
(1)常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_________(填“酸”“碱”或“中”)性,c(CN-)_______(填“>”“<”或“=”)c(HCN)。
(2)常温下,若将c molL-1盐酸与0.61 molL-1KCN溶液等体积混合后恰好得到中性溶液,则c=________(小数点后保留4位数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。化学原理:CH2=CH2(g)+H2O(g)→CH3CH2OH(g)△H。已知几种共价键的键能如下表所示:
化学健 | C-H | C=C | H-O | C-C | C-O |
健能/kJ·mol-1 | 413 | 615 | 463 | 348 | 351 |
下列说法错误的是( )
A. 上述合成乙醇的反应是加成反应
B. 相同时间段内,反应中用三种物质表示的反应速率相等
C. 碳碳双键的键能小于碳碳单键键能的2倍
D. 上述反应式中,△H=-96kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g) ![]() C(g)+D(g),5 min后达到平衡.已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
C(g)+D(g),5 min后达到平衡.已知该温度下其平衡常数K=1,若温度不变时将容器的体积扩大为原来的10倍,A的转化率不发生变化,则( )
A.a=3
B.a=2
C.B的转化率为40%
D.B的转化率为60%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com