
【题目】有一未知的无色溶液,只可能含有以下离子中的若干种:NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、SO42- , 现取两份100mL溶液进行如下实验: ①第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99 g。②第二份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图。以下推测不正确的是( )
A.原溶液一定不存在Cu2+
B.不能确定原溶液是否含有K+
C.实验所加的NaOH的浓度为2mol·L-1
D.原溶液确定含Mg2+、Al3+、NH4+ , 且n(Mg2+) ∶n(Al3+)∶n( NH4+)=1∶1∶1
【答案】D
【解析】A.通过以上分析知,溶液中一定不存在Cu2+ , A不符合题意;
B.当加入40mLNaOH溶液时,剩余的沉淀是Mg(OH)2 , n[Mg(OH)2]=0.01mol,根据原子守恒知,n(Mg2+)=0.01mol,c(Mg2+)= ![]() =0.1mol/L,生成0.01molMg(OH)2需要n(NaOH)是0.02mol,Al(OH)3和NaOH反应生成NaAlO2需要NaOH溶液的体积是5mL,则铝离子和NaOH溶液反应生成Al(OH)3沉淀时需要NaOH溶液的体积是15mL,则生成氢氧化镁需要NaOH溶液的体积是10mL,所以c(NaOH)=
=0.1mol/L,生成0.01molMg(OH)2需要n(NaOH)是0.02mol,Al(OH)3和NaOH反应生成NaAlO2需要NaOH溶液的体积是5mL,则铝离子和NaOH溶液反应生成Al(OH)3沉淀时需要NaOH溶液的体积是15mL,则生成氢氧化镁需要NaOH溶液的体积是10mL,所以c(NaOH)= ![]() =2mol/L,氢氧化铝和NaOH溶液反应生成NaAlO2时,结合原子守恒知,c(Al3+)=
=2mol/L,氢氧化铝和NaOH溶液反应生成NaAlO2时,结合原子守恒知,c(Al3+)= ![]() =0.1mol/L,c(NH4+)=
=0.1mol/L,c(NH4+)= ![]() =0.2mol/L,溶液中c(SO42-)=
=0.2mol/L,溶液中c(SO42-)= ![]() =0.3mol/L,根据溶液中电荷守恒知,3c(Al3+)+c(NH4+)+2(Mg2+)>2c(SO42-),所以溶液中还存在硝酸根离子,不能确定原溶液是否含有K+ , B不符合题意;
=0.3mol/L,根据溶液中电荷守恒知,3c(Al3+)+c(NH4+)+2(Mg2+)>2c(SO42-),所以溶液中还存在硝酸根离子,不能确定原溶液是否含有K+ , B不符合题意;
C.通过B知,c(NaOH)= ![]() =2mol/L,C不符合题意;
=2mol/L,C不符合题意;
D.根据图象知,35-40mL时Al(OH)3和NaOH反应生成NaAlO2 , 则0-25mL时NaOH和Mg2+、Al3+反应生成沉淀,生成NaAlO2时需要NaOH5mL,则生成Al(OH)3需要NaOH 15mL,则有10mLNaOH溶液和镁离子反应,25-35mL时氢氧化钠溶液和NH+4反应生成氨水,根据使用NaOH溶液体积知,n(Mg2+):n(Al3+):n(NH4+)=1:1:2,D符合题意;
故答案为:D根据无色溶液可知,有颜色的离子不能存在,一定不含Cu2+;①第一份加足量BaCl2溶液后,有白色沉淀产生,所以推断一定有SO42-离子;②第二份逐滴滴加NaOH 溶液,由图可知,开始加入氢氧化钠溶液就有沉淀生成,说明不含有H+;沉淀最大时,继续滴加氢氧化钠溶液,沉淀部分溶解,推断一定含有Al3+;图象中有一段平台,说明加入OH-时无沉淀生成,有NH4+ , NH4++OH-=NH3H2O,说明含有铵根离子,最后溶液中有沉淀,说明溶液中含Mg2+;③第一份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g,则溶液中![]() 。据此结合选项进行分析。
。据此结合选项进行分析。


科目:高中化学 来源: 题型:
【题目】体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2 , 在相同温度下发生反应:2SO2+ O2 ![]() 2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3 , 并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
A.等于p%
B.大于p%
C.小于p%
D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一定量的氨基甲酸铵置于密闭真空容器中(固体体积忽略不计)发生反应:H2NCOONH4(s)![]() 2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
2NH3(g)+CO2(g)△H,达到平衡时测得c(CO2)=amol·L-1。温度不变,达到平衡后压缩容器体积至原来的一半,达到新平衡时测得c(NH3)=xmol·L-1。下列说法正确的是( )
A. 混合气体的平均相对分子质量不再变化时表明达到平衡状态
B. 达到新平衡时,△H为原来的2倍
C. 上述反应达到新平衡状态时x=2a
D. 上述反应体系中,压缩容器体积过程中n(H2NCOONH4)不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸入人体內的氧有2%转化为氧化性极强的“活性氧”,它能加速人体衰老,被称为“生命杀手”,服用含硒元素(Se)的化合物亚硒酸钠(Na2SeO3),能消除人体內的活性氧,由此推断 Na2SeO3的作用是( )
A.作还原剂B.作氧化剂C.既作氧化剂又作还原剂D.既不作氧化剂又不作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:C(s)+ ![]() O2(g)=CO(g) ΔH=-110.35kJ·mol-1
O2(g)=CO(g) ΔH=-110.35kJ·mol-1
CO(g)+ ![]() O2(g)=CO2(g) ΔH=-282.57kJ·mol-1
O2(g)=CO2(g) ΔH=-282.57kJ·mol-1
在6 g 碳不完全燃烧所得产物中,CO与CO2的体积比为2∶3, 与6 g碳完全燃烧相比,损失的热量为( )
A.282.57 kJ
B.110.35 kJ
C.196.46 kJ
D.56.51 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物结构简式如图,下列关于该有机物的说法正确的是
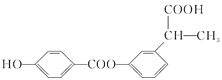
A. 1 mol 该有机物含有 6 mol 碳碳双键
B. 1 mol 该有机物完全燃烧可生成9 mol H2O
C. 1 mol 该有机物可电离生成2 mol H+
D. 1 mol 该有机物最多可与6 mol H2 发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关电解质的说法正确的是
A.固体NaCl不导电,所以NaCl不是电解质
B.SO3水溶液的导电性很好,所以SO3是电解质
C.液态的铜导电性很好,所以铜是电解质
D.Na2O液态时能导电,所以Na2O是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O
(实验内容及部分记录)
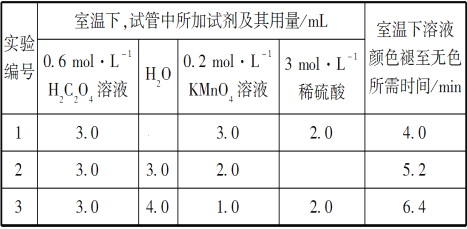
请回答:
(1)根据上表中的实验数据,可以得到的结论是__________________________。
(2)利用实验1中数据计算,用KMnO4的浓度变化表示的反应速率v(KMnO4)=________。
(3)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图甲所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势应如图乙所示。该小组同学根据图乙所示信息提出了新的假设,并继续进行实验探究。
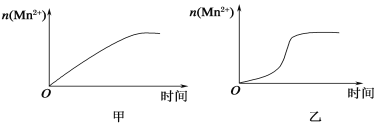
①该小组同学提出的假设是__________________________。
②请你帮助该小组同学完成实验方案,并填写表所加固体的化学式_______。
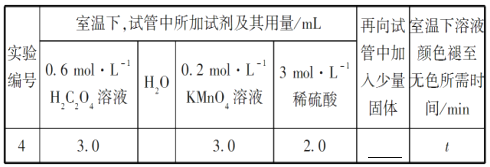
③若该小组同学提出的假设成立,t的大小范围是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关认识正确的是( )
A. 各能级s、p、d、f可容纳的电子数按顺序分别为1、3、5、7的二倍
B. 各能层的能级都是从s能级开始至f能级结束
C. 各能层含有的能级数为n-1
D. 各能层含有的电子数为2n2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com