
| A、C(NH4+)>C(Cl-)>C(H+)>C(OH-) |
| B、C(Cl-)>C(NH4+)>C(OH-)>C(H+) |
| C、C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
| D、C(Cl-)>C(NH4+)>C(H+)>C(OH-) |


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
| A、Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O |
| B、Cu+2FeCl3═CuCl2+2FeCl2 |
| C、HCl+NaHCO3=NaCl+H2O+CO2↑ |
| D、3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:2 | B、3:4 |
| C、1:1 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大量铝土矿 |
| B、电解氧化铝制取铝的方法 |
| C、用金属钠还原氧化铝的方法 |
| D、无水氯化铝与钾制取铝的方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2:3 | B、3:2 |
| C、1:1 | D、1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,11.2L氯气所含的原子数为NA |
| B、常温常压下,1mol氦气含有的核外电子数为4NA |
| C、17g氨气所含的电子数目为10NA |
| D、同温同压下,相同体积的任何气体单质所含的原子数目相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
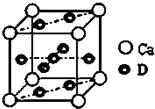 A,B,C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:
A,B,C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com