
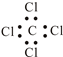
| A、全对 | B、全错 | C、①② | D、③④ |
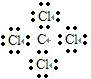 ,故③错误;
,故③错误; 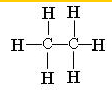 ,故④错误;
,故④错误;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属Na、Mg、Al的硬度依次降低 |
| B、HI、HBr、HCl、HF的稳定性依次减弱 |
| C、干冰、钠、冰的熔点依次降低 |
| D、O、F、H的原子半径依次减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-═Al(OH)3↓ |
| B、碳酸钠溶液中加入澄清石灰水 CO32-+Ca(OH)2+═CaCO3↓+2OH- |
| C、氢氧化钠溶液中通入氯气 Cl2+2OH-═Cl-+ClO-+H2O |
| D、足量稀硝酸中加入铁粉 2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、同温同压下,等质量的甲烷比氖气所占有的体积小 |
| B、3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是64g/mol |
| C、0.5L 1mol/L FeCl3溶液与0.2L 1mol/L KCl溶液中的Cl-的数目之比为15:2 |
| D、100ml 1mol/L NaCl溶液与50ml 1mol/L AlCl3溶液中Cl-物质的量浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.8g重水(D2O)中含NA个中子 |
| B、标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
| C、室温下,14g乙烯和丁烯的混合气体中含有的碳原子数目为NA |
| D、足量的铜与含2molH2SO4的浓硫酸充分反应,可生成NA个SO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO3的电离方程式H2SO3?2H++SO32- |
| B、HCO3-在水溶液中的电离方程式:HCO3-+H2O?H3O++CO32- |
| C、CO32-的水解方程式:CO32-+2H2O?H2CO3+2OH- |
| D、CaCO3的电离方程式:CaCO3?Ca2++CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com