


 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案科目:高中化学 来源: 题型:
| A、1分子H2和Cl2反应,放出热量184.6 kJ |
| B、1 mol H2(g)完全反应生成2 mol HCl(g),放出的热量为184.6 kJ |
| C、在101 kPa、25℃的条件下,1 mol H2(g)和1 mol Cl2(g)完全反应生成2 mol HCl(g)放出的热量为184.6 kJ |
| D、在101 kPa、25℃的条件下,1 mol H2(g)和1 mol Cl2(g)完全反应生成2 mol HCl(g)吸收的热量为184.6 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上用氯气通入纯碱溶液来生产漂白粉 | ||||
B、工业制硫酸的生产过程中,硫元素的转化步骤是:FeS2
| ||||
| C、高炉炼铁的主要反应原理是碳在高温下直接将氧化铁还原成铁 | ||||
| D、在海水中加人石灰乳可得氢氧化镁沉淀,这是从海水中富集镁的基本方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:
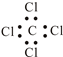
| A、全对 | B、全错 | C、①② | D、③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、根据溶液酸碱性,将化合物分为酸、碱、盐 |
| B、根据分散质微粒直径大小,将分散系分为胶体、浊液和溶液 |
| C、根据元素组成,将物质分为纯净物和混合物 |
| D、根据溶液导电性强弱,将电解质分为强电解质和弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、vA=0.03mol?L-1?min-1 |
| B、vB=0.045 mol?L-1?min-1 |
| C、vC=0.06mol?L-1?min-1 |
| D、vD=0.03 mol?L-1?min-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com